
Neuroscienziati della Georgetown University dicono di aver sviluppato e testato un agente che riduce l'accumulo di proteine tossiche in modelli animali sia di Parkinson che di morbo di Alzheimer (MA), e migliora il comportamento cognitivo e motorio.
Il team ha presentato i risultati sull'agente, il CM101 (chiamato anche BK40143), in una presentazione orale durante la riunione annuale della Society for Neuroscience a Chicago il 22 ottobre.
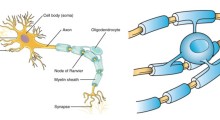
Il CM101 funziona attivando il sistema di “smaltimento dei rifiuti” di un neurone, che è preposto all'eliminazione delle proteine indesiderate e tossiche, come la tau e l'amiloide-beta 42, tra gli altri composti, che spesso si trovano nel MA, e l'alfa-sinucleina, spesso presente nel Parkinson.
“Una dose molto bassa di CM101 attiva lo smaltimento dei rifiuti nei neuroni del cervello per un paio d'ore al giorno, quanto basta per fornire un po' di cibo di proteine neurotossiche nelle cellule. Nel corso del tempo, questo accumulo nei neuroni comincia a sparire“, dice Charbel Moussa MBBS/PhD, professore associato di neurologia alla Georgetown, autore senior dello studio e direttore del Translational Neurotherapeutics Program.
Questo lavoro è una continuazione della ricerca di Moussa sul modo in cui agenti noti come 'inibitori della chinasi tirosina' possono produrre questa reazione e potenzialmente fermare le malattie neurodegenerative. Il suo lavoro ha portato a sperimentazioni cliniche con due farmaci anticancro riproposti, che sono inibitori della chinasi tirosina: nilotinib e Bosutinib.
Questi due farmaci sono somministrati in dosi che per trattare la leucemia e altri tumori del sangue sono fino a 10 volte superiori di quanto è necessario per attivare la pulizia dell'accumulo di proteine nei neuroni.
“L'idea con queste dosi elevate frequenti è che controllare la divisione o proliferazione cellulare, mantenendo funzionante lo smaltimento dei rifiuti, farà incenerire le cellule che si stanno dividendo rapidamente. Queste cellule tumorali cannibalizzeranno se stesse“, dice Alan Fowler, primo autore dello studio e dottorando nel laboratorio di Moussa.
Il nuovo anticipo CM101 riflette la ricerca del laboratorio di Moussa che ha separato i vari percorsi influenzati da diversi inibitori di chinasi tirosina (TK). Gli enzimi TK sono presenti nella maggior parte dei tipi di cellule e hanno molte funzioni, che comprendono la segnalazione, la crescita e la divisione cellulare.
I ricercatori hanno scoperto che nilotinib e Bosutinib inibiscono una serie di diversi TK, tra cui l'Abelson (Abl) e il recettori 1 e 2 del Dominio Discoidin (DDR). Tuttavia, spiega Fowler, test più approfonditi hanno dimostrato che i DDR possono essere le chiavi principali per accendere lo smaltimento dei rifiuti nelle cellule cerebrali colpite da neurodegenerazione.
Il nuovo composto, CM101, progettato e sintetizzato in collaborazione con il professore di chimica Christian Wolf e il suo team alla Georgetown, si concentra in particolare sulla inibizione di DDR1 e 2.
“Stiamo riproponendo farmaci inibitori di TK verso le malattie neurodegenerative; la stragrande maggioranza delle quali presentano accumulo tossico nelle cellule cerebrali”, spiega Moussa. “I nostri studi suggeriscono che questa strategia funziona nei neuroni che sono malati, ma che hanno una vitalità residua sufficiente per essere riprogrammati”.
Sia nilotinib che Bosutinib sono oggetto di studio in esperimenti clinici con persone con malattie neurodegenerative. Moussa ha aggiunto:
“Questo agente è stato sottoposto a test in diversi modelli animali di neurodegenerazione, e rappresenta un buon candidato che deve essere studiato in sperimentazioni umane. Finora abbiamo dimostrato che questo agente ha un'efficacia superiore a respingere proteine neurotossiche negli animali rispetto ad agenti simili, e abbiamo identificato i DDR come bersaglio farmacologico preferenziale e ottimale. Il passo successivo è indagare sulla tossicità del farmaco per ottenere l'autorizzazione regolamentare per l'applicazione umana“.
Fonte: Georgetown University (> English text) - Traduzione di Franco Pellizzari.
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.




 Associazione Alzheimer OdV
Associazione Alzheimer OdV