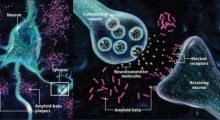
L'Alzheimer è caratterizzato da proteine anomale che si attaccano insieme in piccoli grumi, interrompendo le funzioni cognitive (pensiero, apprendimento e memoria), per lo più composte da peptide beta-amiloide.
Una migliore comprensione di queste proteine, come si formano e come influenzano la funzione del cervello, potrà senza dubbio migliorare la diagnosi e il trattamento della malattia.
A tal fine, un gruppo di ricerca guidato da Stuart A. Lipton, MD, Ph.D, del Sanford-Burnham Medical Research Institute (Sanford-Burnham) hanno trovato che la distruzione delle sinapsi (le connessioni che mediano la comunicazione tra le cellule nervose) indotta dal beta-amiloide, è guidata da una modificazione chimica di un enzima chiamato Cdk5. Il team ha scoperto che questa forma alterata di Cdk5 (SNO-Cdk5) era prevalente nel cervello umano di Alzheimer, ma non nel cervello normale. Questi risultati, pubblicati online nella settimana del 15 agosto nei AProceedings of the National Academy of Sciences, suggeriscono che il SNO-Cdk5 potrebbe essere un obiettivo per lo sviluppo di nuove terapie della malattia di Alzheimer.
Il Cdk5 è un enzima noto per svolgere un ruolo nella normale sopravvivenza e migrazione neuronale. In questo studio, il Dott. Lipton e colleghi hanno scoperto che il peptide beta-amiloide, il segno distintivo dell'Alzheimer, scatena modifiche del Cdk5 con un processo chimico chiamato S-nitrosilazione. In questa reazione, l'ossido nitrico (NO) si attacca all'enzima, producendo SNO-Cdk5 e interrompendo la sua normale attività.
"Dopo che il NO si è attaccato al Cdk5, salta poi come una 'patata bollente' a un'altra proteina chiamata Drp1, interrompendone la funzione e frammentando i mitocondri, la centrale energetica delle cellule nervose. Quando i mitocondri sono danneggiati, le sinapsi, che normalmente richiedono molta energia per la loro funzione, vengono distrutte. Questo scenario interrompe la comunicazione tra le cellule nervose, e quindi la memoria e le capacità cognitive nell'Alzheimer", ha detto il Dott. Lipton, professore e direttore del Centro Del E. Webb Neuroscience, Aging and Stem Cell Research della Sanford-Burnham. Il dottor Lipton è anche un neurologo che vede pazienti con Alzheimer nella sua pratica clinica, ed è accreditato per la caratterizzazione e lo sviluppo della memantina (Namenda ®), l'ultimo farmaco approvato dalla FDA per l'Alzheimer.
In questo studio, il Cdk5 dimostra di svolgere una nuova funzione non nota in precedenza: la possibilità di trasferire NO da una proteina all'altra. Fino ad ora, il Cdk5 era conosciuto solo per l'influenza della funzione di altre proteine attaccandole ai gruppi di fosfato in un processo noto come fosforilazione. Il nuovo studio mostra che l'aggiunta di NO manda il Cdk5 in super azione e gli permette anche di S-nitrosylatare altre proteine, in questo caso la Drp1, sui mitocondri. In particolare, il trasferimento di NO dal SNO-Cdk5 alla Drp1 scatena una perdita di sinapsi, la parte di cellula nervosa che trasmette i segnali elettrochimici ad altre cellule nervose. La perdita di sinapsi è nota per essere correlata al grado di declino cognitivo nell'Alzheimer.
Portando lo studio un ulteriore passo avanti, il team ha confrontato i livelli di SNO-Cdk5 nel tessuto cerebrale di soggetti sani e di pazienti affetti da Alzheimer. Il SNO-Cdk5 era drasticamente più elevato nel cervello umano con Alzheimer. "I nostri esperimenti fatti utilizzando tessuti umani di cervello di pazienti con Alzheimer danno a questo dato una chiara rilevanza clinica", ha detto il Dott. Lipton. "Il SNO-Cdk5 potrebbe fornire un nuovo bersaglio per il trattamento di questa malattia devastante".
Ben 5,3 milioni di americani vivono con l'Alzheimer, attualmente la settima causa di morte negli Stati Uniti. Questo studio è stato finanziato dai National Institutes of Health (NIH). Co-autori: Jing Qu, Tomohiro Nakamura, Gang Cao, Emily A. Holland, Scott R. McKercher, e Stuart A. Lipton, tutti della Sanford-Burnham a La Jolla, in California.
Cosa pensi di questo articolo? Ti è stato utile? Hai rilievi, riserve, integrazioni? Conosci casi o ti è successo qualcosa che lo conferma? o lo smentisce?
Puoi usare il modulo dei commenti sotto per dire la tua opinione. Che è importante e unica. Non tenerla per te, non farci perdere l'occasione di conoscerla.
Fonte: Materiale del Sanford-Burnham Medical Research Institute, via EurekAlert!, un servizio di AAAS.
Riferimento: Jing Qu, Tomohiro Nakamura, Gang Cao, Emily A. Holland, Scott R. McKercher, and Stuart A. Lipton. S-Nitrosylation activates Cdk5 and contributes to synaptic spine loss induced by β-amyloid peptide. Proceedings of the National Academy of Sciences, August 15, 2011 DOI: 10.1073/pnas.1105172108.
Pubblicato in ScienceDaily il 16 Ago 2011 - Traduzione di Franco Pellizzari.
Copyright: Tutti i diritti di eventuali testi o marchi, eventualmente citati nell'articolo, sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non si propone come terapia o dieta; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer Riese. I siti terzi raggiungibili dagli annunci pubblicitari proposti da Google sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente; in particolare si segnala la presenza frequente di una istituzione medica con base in Germania (xcell-Center) che propone la cura dell'Alzheimer con cellule staminali; la Società Tedesca di Neuroscienze ha più volte messo in guardia da questa proposta il cui effetto non è dimostrato. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.| Sostieni l'Associazione, una donazione, anche minima, ci aiuterà ad assistere malati e famiglie e a informarti: |







 Associazione Alzheimer OdV
Associazione Alzheimer OdV