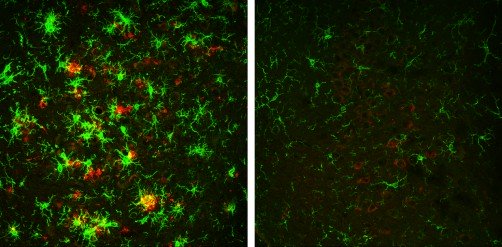
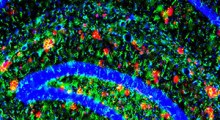
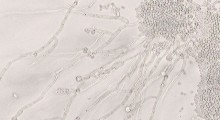
 Il cervello di un topo di 10 mesi con Alzheimer (a sinistra) è pieno di placche amiloidi (rosse) circondate da microglia attive (verde). Ma questi segni distintivi del morbo sono invertiti negli animali che hanno gradualmente perso l'enzima BACE1 (a destra). Fonte: Hu et al., 2018 Un team di ricercatori del Lerner Research Institute della Cleveland Clinic ha scoperto che rimuovendo gradualmente un enzima chiamato BACE1, si inverte completamente la formazione di placche di amiloide nel cervello dei topi con morbo di Alzheimer (MA), migliorando così la funzione cognitiva degli animali.
Il cervello di un topo di 10 mesi con Alzheimer (a sinistra) è pieno di placche amiloidi (rosse) circondate da microglia attive (verde). Ma questi segni distintivi del morbo sono invertiti negli animali che hanno gradualmente perso l'enzima BACE1 (a destra). Fonte: Hu et al., 2018 Un team di ricercatori del Lerner Research Institute della Cleveland Clinic ha scoperto che rimuovendo gradualmente un enzima chiamato BACE1, si inverte completamente la formazione di placche di amiloide nel cervello dei topi con morbo di Alzheimer (MA), migliorando così la funzione cognitiva degli animali.
Lo studio, pubblicato ieri 14 febbraio sul Journal of Experimental Medicine, fa sorgere la speranza che i farmaci che prendono di mira questo enzima riescano a trattare con successo il MA negli esseri umani.
Uno dei primi eventi del MA è un accumulo anomalo di peptide amiloide-beta, che può formare grandi placche amiloidi nel cervello e interrompere la funzione delle sinapsi neuronali. Il BACE1, chiamato anche beta-secretasi, aiuta a produrre il peptide amiloide-beta mediante la scissione della 'proteina precursore dell'amiloide' (APP). Come potenziali trattamenti per il MA sono quindi sviluppati dei farmaci che inibiscono il BACE1, ma, poiché il BACE1 controlla molti processi importanti attraverso la scissione di proteine diverse dall'APP, questi farmaci potrebbero avere seri effetti collaterali.
I topi completamente privi di BACE1 soffrono di gravi difetti nel neurosviluppo. Per capire se l'inibizione del BACE1 negli adulti potrebbe essere meno dannoso, Riqiang Yan e colleghi hanno generato topi che perdono gradualmente questo enzima via via che invecchiano. Questi topi si sono sviluppati normalmente e sembravano rimanere perfettamente sani nel tempo.
I ricercatori hanno poi incrociato questi roditori con topi che iniziano a sviluppare placche amiloidi e MA quando hanno 75 giorni. Anche la progenie risultante ha formato placche a questa età, pur se i loro livelli di BACE1 erano inferiori al normale di circa il 50%. Sorprendentemente, tuttavia, le placche hanno cominciato a scomparire quando i topi continuavano ad invecchiare e perdevano l'attività del BACE1, fino a quando, a 10 mesi di età, i topi non avevano affatto placche nel cervello.
"A nostra conoscenza, questa è la prima osservazione di un'inversione così drastica della deposizione di amiloide in qualsiasi studio sui topi modello di MA", dice Yan, che questa primavera si trasferirà all'Università del Connecticut come preside del dipartimento di neuroscienze.
La riduzione dell'attività del BACE1 ha anche determinato livelli più bassi di peptide amiloide-beta e ha invertito altri segni distintivi del MA, come l'attivazione delle cellule microgliali e la formazione di processi neuronali anomali. La perdita di BACE1 ha anche migliorato l'apprendimento e la memoria dei topi con MA.
E tuttavia, quando i ricercatori hanno fatto registrazioni elettrofisiologiche dei neuroni di questi animali, hanno scoperto che l'esaurimento del BACE1 ha ripristinato solo parzialmente la funzione sinaptica, suggerendo che il BACE1 potrebbe essere richiesto per un'attività sinaptica e una cognizione ottimale.
"Il nostro studio fornisce prove genetiche che la deposizione di amiloide preformata può essere completamente invertita con la deplezione sequenziale e aumentata di BACE1 nell'adulto", afferma Yan. "I nostri dati mostrano che gli inibitori del BACE1 hanno il potenziale di trattare i pazienti con Alzheimer senza tossicità indesiderata. Studi futuri dovrebbero sviluppare strategie per ridurre al minimo i deficit sinaptici derivanti da una significativa inibizione del BACE1, per dare il massimo di benefici ai malati di Alzheimer".
Fonte: Rockefeller University Press via Newswise (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Xiangyou Hu, Brati Das, Hailong Hou, Wanxia He, Riqiang Yan. BACE1 deletion in the adult mouse reverses preformed amyloid deposition and improves cognitive functions. The Journal of Experimental Medicine, 2018; jem.20171831 DOI: 10.1084/jem.20171831
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.







 Associazione Alzheimer OdV
Associazione Alzheimer OdV