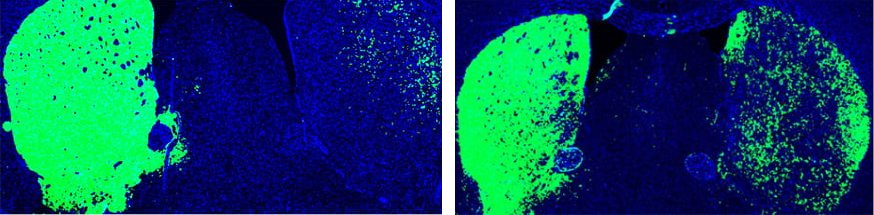
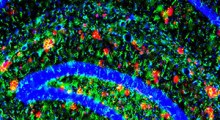
 Sinistra: cervello di topo prima della riprogrammazione, con i neuroni dopaminergici in verde. Destra: cervello di topo dopo la riprogrammazione con il trattamento oligonucleotide antisenso PTB, che ha convertito gli astrociti in neuroni dopaminergici (verdi).
Sinistra: cervello di topo prima della riprogrammazione, con i neuroni dopaminergici in verde. Destra: cervello di topo dopo la riprogrammazione con il trattamento oligonucleotide antisenso PTB, che ha convertito gli astrociti in neuroni dopaminergici (verdi).
Xiang-Dong Fu PhD, non è mai stato così entusiasta di qualcosa in tutta la sua carriera. Ha studiato a lungo la biologia di base dell'RNA, un cugino genetico del DNA e delle proteine che lo legano. Ma una singola scoperta ha lanciato Fu in un campo completamente nuovo: le neuroscienze.
Da decenni, Fu e il suo team dell'Università della California di San Diego stanno studiando una proteina chiamata PTB, che è ben nota per legare l'RNA e influenzare quali geni sono accesi o spenti in una cellula. Per studiare il ruolo di una proteina come la PTB, gli scienziati spesso manipolano le cellule per ridurre la quantità di quella proteina, e poi vedere cosa succede.
Diversi anni fa, un ricercatore post-dottorato del laboratorio di Fu stava usando questo approccio, con una tecnica chiamata siRNA per silenziare il gene PTB in cellule del tessuto connettivo chiamate fibroblasti. Ma è un processo noioso che deve essere eseguito più e più volte. Dopo essersi stancato ha convinto Fu che avrebbero dovuto usare una tecnica diversa per creare una linea cellulare stabile che manca in permanenza della PTB. In un primo momento, il ricercatore si è lamentato anche di questa nuova tecnica, perché faceva crescere le cellule troppo lentamente.
Ma dopo un paio di settimane ha notato qualcosa di strano: erano rimasti pochissimi fibroblasti, quasi tutto il piatto era invece pieno di neuroni. In questo modo fortuito, il team ha scoperto che l'inibizione o l'eliminazione di un singolo gene (quello che codifica la PTB) trasforma diversi tipi di cellule del topo direttamente in neuroni.
Più di recente, Fu e Hao Qian PhD, un altro ricercatore post-dottorato nel suo laboratorio, hanno fatto fare alla scoperta un grande passo in avanti, applicandola in quello che potrebbe un giorno essere un nuovo approccio terapeutico per il Parkinson e per altre malattie neurodegenerative. Un solo trattamento, che ha inibito la PTB nei topi, è stato sufficiente a convertire astrociti nativi (cellule di supporto a forma di stella del cervello) in neuroni che producono il neurotrasmettitore dopamina. Di conseguenza, nei topi sono scomparsi i sintomi del Parkinson.
Lo studio è pubblicato il 24 giugno 2020 su Nature.
“I ricercatori di tutto il mondo hanno cercato molti modi per generare neuroni in laboratorio, usando cellule staminali e altri mezzi, così da studiarli meglio, e usarli per sostituire i neuroni persi nelle malattie neurodegenerative”, ha detto Fu, professore di medicina molecolare e cellulare alla UC San Diego. “Il fatto che siamo riusciti a produrre tanti neuroni in modo relativamente facile è stata una grande sorpresa”.
Ci sono diversi modi per imitare il Parkinson nei topi. In questo caso, i ricercatori hanno applicato una molecola che assomiglia alla dopamina per avvelenare i neuroni che producono la dopamina. Come risultato, i topi perdono i neuroni che producono dopamina e sviluppano sintomi simili al Parkinson, come ad esempio le deficienze di movimento.
Il trattamento funziona così: i ricercatori hanno sviluppato un virus non-infettivo che porta una sequenza oligonucleotide antisenso, un pezzo artificiale di DNA progettato per legarsi specificamente all'RNA che codifica la PTB, così da degradarlo, impedire che sia tradotto in una proteina funzionale e che stimoli lo sviluppo dei neuroni.
Gli oligonucleotidi antisenso, chiamati anche farmaci di progettazione del DNA, sono un approccio collaudato per le malattie neurodegenerative e neuromuscolari; il coautore dello studio, Don Cleveland PhD, è il pioniere della tecnologia, che ora costituisce la base della terapia approvata dalla Food and Drug Administration per l'atrofia muscolare spinale e di molte altre terapie attualmente in sperimentazione clinica. Cleveland è preside del Dipartimento di Medicina Molecolare e Cellulare della UC San Diego e fa parte del Ludwig Institute for Cancer Research.
I ricercatori hanno somministrato il trattamento con oligonucleotidi antisenso PTB direttamente al mesencefalo del topo, dove avviene la regolazione del controllo motorio e dei comportamenti di ricompensa, la parte del cervello che di solito perde i neuroni che producono dopamina nel Parkinson. Un gruppo di controllo di topi ha ricevuto un trattamento finto con un virus vuoto o una sequenza antisenso irrilevante.
Nei topi trattati, un piccolo sottoinsieme di astrociti si è convertito in neuroni, aumentando il numero di neuroni di circa il 30%. I livelli di dopamina si sono ripristinati ad un livello paragonabile a quello dei topi normali. Ancora di più, i neuroni sono cresciuti e hanno inviato i loro processi in altre parti del cervello. Nei topi di controllo invece non c'è stato alcun cambiamento.
Su due diverse misurazioni di movimento e risposta degli arti, i topi trattati sono tornati alla normalità entro tre mesi dopo un singolo trattamento, e sono rimasti completamente privi di sintomi di Parkinson per il resto della loro vita. Al contrario, i topi di controllo non hanno mostrato alcun miglioramento.
“Sono rimasto sbalordito da quello che ho visto”, ha detto il co-autore William Mobley MD/PhD, professore di neuroscienze della UC San Diego. “Tutta questa nuova strategia per il trattamento della neurodegenerazione dà speranza che sia possibile aiutare anche quelli con la malattia avanzata”.
Cosa ha a che fare la PTB con questo effetto? “Questa proteina è presente in molte cellule”, ha detto Fu. “Ma, quando i neuroni cominciano a svilupparsi dai loro precursori, essa scompare naturalmente. Quello che abbiamo trovato è che costringere la PTB ad andare via è l'unico segnale di cui una cellula ha bisogno per accendere i geni necessari per produrre un neurone”.
Naturalmente, i topi non sono persone, ha ammonito. Il modello usato dal team non riassume perfettamente tutte le caratteristiche essenziali del Parkinson. Ma lo studio fornisce una prova di concetto, ha detto Fu.
Per il seguito, il team ha in programma di ottimizzare i suoi metodi e testare l'approccio in topi modello che imitano il Parkinson attraverso cambiamenti genetici. Essi hanno anche brevettato il trattamento con oligonucleotide antisenso PTB, per procedere ai test negli esseri umani.
“Il mio sogno è vedere questo nella sperimentazione clinica, per testare questo approccio come trattamento per il Parkinson, ma anche per molte altre malattie in cui si perdono i neuroni, come l'Alzheimer, il morbo di Huntington e l'ictus”, ha detto Fu. “E sognando ancora più in grande, cosa succederebbe se potessimo puntare la PTB per correggere difetti in altre parti del cervello, per trattare cose come i difetti cerebrali ereditari? Voglio passare il resto della mia carriera a rispondere a queste domande”.
Fonte: Heather Buschman PhD in University of California San Diego (> English text) - Traduzione Franco Pellizzari.
Riferimenti: Hao Qian, Xinjiang Kang, Jing Hu, Dongyang Zhang, Zhengyu Liang, Fan Meng, Xuan Zhang, Yuanchao Xue, Roy Maimon, Steven F. Dowdy, Neal K. Devaraj, Zhuan Zhou, William C. Mobley, Don W. Cleveland, Xiang-Dong Fu. Reversing a model of Parkinson’s disease with in situ converted nigral neurons. Nature, 2020, DOI
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.



 Associazione Alzheimer OdV
Associazione Alzheimer OdV