Parlando di Alzheimer, si dice di solito che il Golgi sia uno spettatore vittima. Nuove scoperte dicono invece che curare il Golgi rallenta significativamente l'accumulo delle proteine di AD.
 L'Alzheimer (AD) avanza all'interno del cervello in una tempesta crescente di caos cellulare, quando i depositi della proteina tossica amiloide-beta (Aβ) sopraffanno i neuroni.
L'Alzheimer (AD) avanza all'interno del cervello in una tempesta crescente di caos cellulare, quando i depositi della proteina tossica amiloide-beta (Aβ) sopraffanno i neuroni.
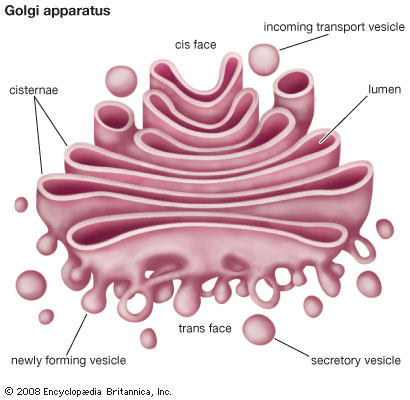
Un effetto collaterale apparente dell'accumulo di Aβ nei neuroni è la frammentazione del Golgi, la parte della cellula coinvolta nell'imballaggio e nello smistamento dei carichi di proteine, compreso il precursore dell'Aβ.
Ma la distruzione del Golgi è una sorta di danno collaterale della tempesta di Aβ, o è la perdita delle funzioni dell'apparato Golgi ad indurre l'Alzheimer?
Questa era la domanda di fronte a Yanzhuang Wang, Gunjan Joshi, ed i loro colleghi dell'Università del Michigan di Ann Arbor, quando si sono prefissati di scoprire il meccanismo che danneggia il Golgi, usando un topo transgenico e delle colture di tessuti modelli di AD per esaminare quello che succede.
La parte sorprendente della risposta è che i livelli crescenti di Aβ non portano direttamente alla frammentazione del Golgi attivando la chinasi del ciclo cellulare cdk5. Altrettanto sorprendente è stato che la funzione del Golgi può essere recuperata bloccando la cdk5 o schermando la sua proteina bersaglio a valle nel Golgi, la GRASP65.
La risposta ancora più sorprendente è che il recupero del Golgi riduce significativamente l'accumulo di Aβ, apparentemente riaprendo un normale percorso di degradazione proteico per la proteina precursore dell'amiloide (APP). A Wang et al, questo suggerisce una nuova linea di attacco per i farmaci nella speranza di rallentare la progressione dell'AD.
Parlando al Meeting BCSA/IFCB di Filadelfia, i ricercatori hanno detto che la frammentazione del Golgi è di per sé un meccanismo importante, e fino ad oggi sconosciuto, attraverso il quale l'Aβ estende i suoi effetti tossici. Essi ritengono che, quando sale l'accumulo di Aβ, aumentano i danni ai Golgi, che a loro volta accelerano il traffico di APP, determinando l'aumento della produzione di Aβ.
Questo è un classico «circuito deleterio di retroazione», dicono. Bloccando la cdk5 o il suo obiettivo a valle, questo circuito può essere spezzato o fortemente rallentato. "Il nostro studio fornisce un meccanismo molecolare della frammentazione del Golgi e dei suoi effetti sul traffico e sull'elaborazione della APP in AD, suggerendo che il Golgi può essere un bersaglio potenziale di farmaci per il trattamento dell'AD", concludono i ricercatori del Michigan.
Fonte: American Society for Cell Biology via Newswise (> English text) - Traduzione di Franco Pellizzari.
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer onlus di Riese Pio X. I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.
| Sostieni l'Associazione; una donazione, anche minima, ci aiuterà ad assistere malati e famiglie e continuare ad informarti. Clicca qui a destra: |





 Associazione Alzheimer OdV
Associazione Alzheimer OdV