Nuova tecnologia CRISPR rimette in pista le microglia malate.
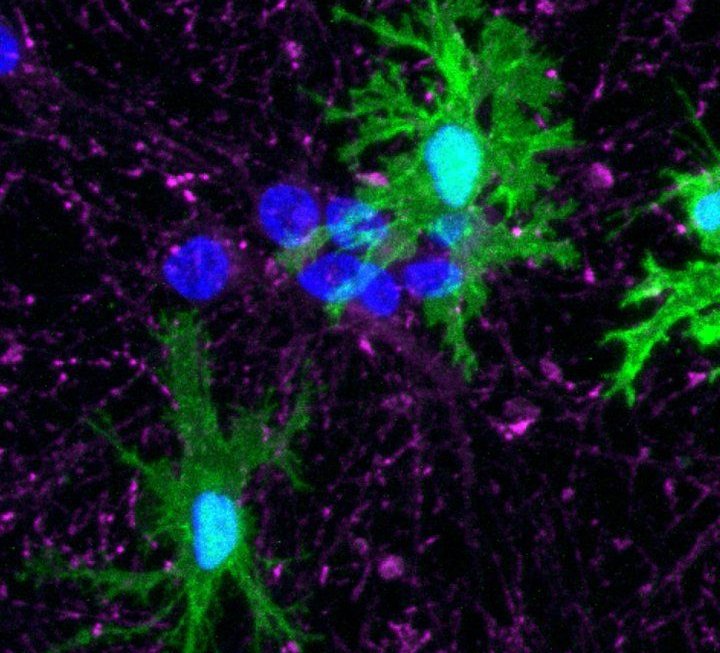 Microglia (verdi) ottenute da cellule staminali umane dal laboratorio Kampmann. (Fonte: Olivia Teter)
Microglia (verdi) ottenute da cellule staminali umane dal laboratorio Kampmann. (Fonte: Olivia Teter)
La scoperta del modo di cambiare le cellule cerebrali danneggiate da uno stato malato a uno sano presenta un nuovo percorso potenziale per trattare il morbo di Alzheimer (MA) e altre forme di demenza. Un nuovo studio di ricercatori della University of California di San Francisco si è concentrato sulle microglia, le cellule che stabilizzano il cervello eliminando i neuroni danneggiati e le placche proteiche spesso associate alla demenza e ad altre malattie cerebrali.
"Queste cellule sono poco studiate, nonostante sia noto che i cambiamenti che le interessano abbiano un ruolo significativo nel MA e in altre malattie cerebrali", ha affermato Martin Kampmann PhD, autore senior nello studio, apparso l'11 agosto su Nature Neuroscience. "Ora, usando un nuovo metodo CRISPR che abbiamo sviluppato, possiamo controllare effettivamente queste microglia, perché smettano di fare cose tossiche e tornino a svolgere i loro lavori vitali di pulizia. Questa capacità offre l'opportunità di un tipo di approccio terapeutico completamente nuovo".
Sfruttare il sistema immunitario del cervello
La maggior parte dei geni noti per aumentare il rischio di MA agisce attraverso le microglia. Pertanto, queste cellule hanno un impatto significativo sul modo di manifestarsi di tali malattie neurodegenerative, ha affermato Kampmann.
Le microglia fungono da sistema immunitario del cervello. Le cellule immunitarie ordinarie non possono attraversare la barriera emato-encefalica, quindi è compito delle microglia sane eliminare i rifiuti e le tossine, mantenendo i neuroni funzionanti al meglio. Quando le microglia iniziano a perdere il loro percorso, il risultato può essere l'infiammazione cerebrale e il danno ai neuroni e alle reti che formano.
In alcune condizioni, ad esempio, le microglia iniziano a rimuovere le sinapsi tra i neuroni: sebbene questa sia una parte normale dello sviluppo del cervello nell'infanzia e nell'adolescenza, può avere effetti disastrosi nel cervello adulto.
All'incirca negli ultimi 5 anni, molti studi hanno osservato e profilato questi stati microgliali diversi, ma non sono stati in grado di caratterizzare la genetica che li sottende. Kampmann e il suo team volevano identificare esattamente quali geni sono coinvolti in specifici stati di attività microgliale e come è regolato ciascuno di questi stati. Con questa conoscenza, sono quindi riusciti a spegnere e attivare i geni, riportando le cellule ribelli sulla strada giusta.
Dalla genomica avanzata a un santo graal
Per realizzare quell'attività i ricercatori hanno dovuto superare ostacoli fondamentali che finora avevano impedito di controllare l'espressione genica in queste cellule. Ad esempio, le microglia sono molto resistenti alla tecnica CRISPR più comune, che prevede di trarre il materiale genetico desiderato dalla cellula usando un virus per il trasporto.
Per ovviare a questo, il team di Kampmann ha convinto delle cellule staminali donate da volontari umani a diventare microglia e hanno ottenuto la conferma che queste cellule funzionassero come le loro normali controparti umane. Il team ha quindi sviluppato una nuova piattaforma che combina una forma di CRISPR, che consente ai ricercatori di attivare e spegnere i singoli geni - e che Kampmann ha contribuito in modo significativo a sviluppare - con letture di dati che indicano funzioni e stati delle singole microglia.
Attraverso questa analisi, Kampmann e il suo team hanno individuato i geni che influenzano la capacità della cellula di sopravvivere e proliferare, la sua propensione a produrre sostanze infiammatorie e l'aggressività con cui pota le sinapsi. E, visto che gli scienziati avevano determinato quali geni controllano tali attività, erano in grado di ripristinare i geni e rimettere la cellula malata in uno stato sano.
Armato di questa nuova tecnica, Kampmann prevede di indagare su come controllare gli stati pertinenti delle microglia, puntando le cellule con molecole farmaceutiche esistenti e testandole in modelli preclinici (=animali). Spera di trovare molecole specifiche che agiscono sui geni necessari per riportare le cellule malate a uno stato sano.
Kampmann ha affermato che una volta invertiti i geni giusti, è probabile che le microglia 'riparate' riprenderanno le loro responsabilità, rimuovendo le placche associate alla malattia neurodegenerativa e proteggendo le sinapsi anziché farle a pezzi.
"Il nostro studio fornisce un progetto per un nuovo approccio al trattamento", ha affermato. "È un po' un santo graal".
Fonte: Robin Marks in University of California - San Francisco (> English) - Traduzione di Franco Pellizzari.
Riferimenti: Nina Dräger, ...[+17], Martin Kampmann. A CRISPRi/a platform in human iPSC-derived microglia uncovers regulators of disease states. Nature Neuroscience, 11 Aug 2022, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.





 Associazione Alzheimer OdV
Associazione Alzheimer OdV