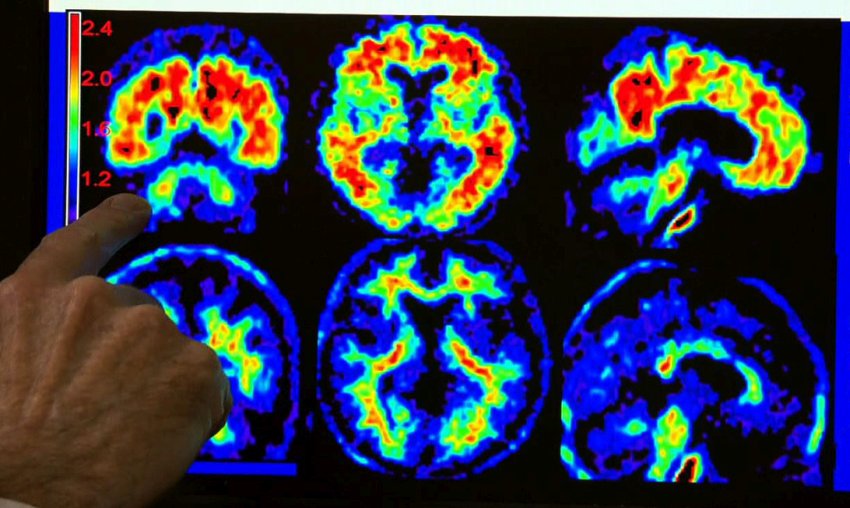
Le mutazioni del gene TREM2 possono aumentare significativamente il rischio di morbo di Alzheimer (MA). Gli scienziati del Centro Tedesco Malattie Neurodegenerative (DZNE) e dell'Università Ludwig-Maximilians di Monaco di Baviera fanno ora luce sui motivi per cui il TREM2 è così importante per la salute del cervello.
Mostrano che il TREM2 attiva le cellule immunitarie del cervello che eliminano i depositi tossici, anzitutto nelle prime fasi della malattia. Lo studio è pubblicato sulla rivista Nature Neuroscience e ha importanti implicazioni per lo sviluppo di nuovi farmaci.
Una caratteristica del MA è la formazione di depositi tossici nel cervello, le cosiddette placche. Le cellule immunitarie specializzate chiamate microglia proteggono il cervello liberandolo da questi detriti tossici. Il TREM2 è un fattore chiave nell'attivazione della microglia e può essere quindi un obiettivo importante per nuovi approcci terapeutici.
Per esplorare ulteriormente queste opzioni terapeutiche, gli scienziati di Monaco di Baviera hanno effettuato un'analisi dettagliata dello sviluppo della malattia nei topi con e senza un gene TREM2 funzionale. Nei topi con TREM2 sano, le microglia si raggruppano attorno alle piccole placche che emergono all'inizio del processo patologico e impediscono loro di ingrandirsi o diffondersi.
"Siamo riusciti a dimostrare che le microglia sono specificamente attratte dalle placche amiloidi, circondano le singole placche e le inghiottono pezzo per pezzo", spiega il capo ricercatore Christian Haass, portavoce del sito DZNE di Monaco, e professore dell'Università Ludwig-Maximilians di Monaco. Al contrario, nei topi privi di TREM2, la microglia non è in grado di svolgere questo importante compito. L'attivazione terapeutica di TREM2 in uno stadio precoce della malattia potrebbe quindi aiutare a contrastare la formazione di aggregati tossici di proteine amiloide-beta.
Tuttavia, i risultati dello studio richiedono anche cautela nell'implementazione di tale terapia. Mentre il TREM2 previene la formazione della placca alla partenza della malattia, potrebbe avere l'effetto opposto in seguito. Nelle fasi più avanzate della malattia, le placche crescevano più velocemente nei topi con TREM2 funzionale rispetto ai topi privi del gene corrispondente.
I ricercatori hanno scoperto che questo potrebbe essere spiegato dal fatto che il TREM2 induce la microglia a produrre una sostanza chiamata ApoE, che enfatizza la formazione di aggregati. "Il nostro studio dimostra che dobbiamo essere estremamente attenti e studiare a fondo un nuovo approccio terapeutico in modelli animali prima di testarlo sugli esseri umani", dice Haass. "Secondo i nostri risultati, potrebbero esserci conseguenze drammatiche se si eccita la microglia".
"In futuro, sarà importante trattare il MA in modo specifico alla fase", spiega Haass. Secondo il presente studio, ad esempio, l'attivazione della microglia tramite TREM2 sarebbe una strategia che dovrebbe essere applicata precocemente nella progressione della malattia.
Haass e i suoi colleghi stanno attualmente lavorando allo sviluppo di anticorpi che stabilizzano il TREM2 e quindi attivano la microglia. Gli scienziati stanno ora usando diversi modelli animali e diversi approcci sperimentali per testare possibili strategie terapeutiche e terapie combinate con altri farmaci.
"Tutte le alterazioni genetiche importanti che aumentano il rischio di MA portano a cambiamenti nella formazione della placca", spiega Haass. Questo suggerisce che questi aggregati proteici sono la causa della malattia. L'attuale studio fornisce la speranza che sia possibile contrastare la formazione della placca attivando il TREM2, e al tempo stesso evidenzia i potenziali rischi che gli scienziati devono prendere in considerazione quando si persegue tale approccio.
Fonte: DZNE (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Samira Parhizkar et al. Loss of TREM2 function increases amyloid seeding but reduces plaque-associated ApoE. Nature Neuroscience, 7 Jan 2019, DOI: 10.1038/s41593-018-0296-9
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.




 Associazione Alzheimer OdV
Associazione Alzheimer OdV