Un sistema innovativo di coltura in laboratorio è riuscito, per la prima volta, a riprodurre l'intero corso degli eventi che sta alla base dello sviluppo dell'Alzheimer.
Con il sistema che hanno sviluppato, i ricercatori della Genetics e Aging Research Unit del Massachusetts General Hospital (MGH) hanno ora la prima chiara evidenza a supporto dell'ipotesi che la deposizione di placche di amiloide-beta nel cervello è la prima di una serie di fasi che portano alla malattia neurodegenerativa devastante.
Essi hanno anche identificato il ruolo essenziale in questo processo di un enzima, la cui inibizione potrebbe essere un bersaglio terapeutico.
"L'ipotesi amiloide, avanzata inizialmente alla metà degli anni '80, sostiene che i depositi di amiloide-beta nel cervello inducono tutti gli eventi successivi: i grovigli neurofibrillari che soffocano l'interno dei neuroni, la morte delle cellule neuronali, e l'infiammazione che porta ad un circolo vizioso di massiccia morte cellulare", dice Rudolph Tanzi, PhD, direttore della Genetics and Aging Research Unit del MGH e co-autore senior del rapporto pubblicato online su Nature. "Da allora ci siamo sempre chiesti se è l'amiloide-beta che in realtà innesca la formazione dei grovigli che uccidono i neuroni. In questo nuovo sistema che noi chiamiamo «Alzheimer-in-un-piatto», siamo riusciti di dimostrare per la prima volta che la deposizione di amiloide è sufficiente a portare ai grovigli e di conseguenza alla morte cellulare".
Anche se i modelli di topi di Alzheimer, che esprimono le varianti del gene che causa la forma ad esordio precoce ereditaria della malattia, sviluppano placche amiloidi nel cervello e deficit di memoria, non hanno i grovigli neurofibrillari che causano la maggior parte dei danni. Altri modelli riescono a produrre grovigli ma non placche. I neuroni in coltura di pazienti umani con Alzheimer hanno livelli elevati della forma tossica di amiloide presente nelle placche e la versione anomala della proteina tau che compone i grovigli, ma non vere placche e grovigli.
Il ricercatore Doo Yeon Kim, PhD, della Genetics and Aging Research Unit, co-autore senior dello studio su Nature, si è reso conto che i sistemi bidimensionali liquidi, usati di solito per coltivare cellule in coltura, rappresentano poco l'ambiente tridimensionale gelatinoso all'interno del cervello. Al contrario il team del MGH ha usato un sistema di coltura tridimensionale a base di gel per allevare cellule umane staminali neurali portatrici di varianti in due geni (la proteina precursore dell'amiloide e la presenilina 1) note per essere alla base dell'Alzheimer familiare ad esordio precoce (FAD). Entrambi questi geni sono stati scoperti anche nel laboratorio di Tanzi.
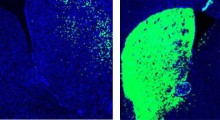
Dopo essere cresciute per sei settimane, le cellule FAD-varianti hanno esibito significativi incrementi sia della forma tipica dell'amiloide-beta che della forma tossica associata all'Alzheimer. Le cellule varianti contenevano anche i grovigli neurofibrillari che soffocano l'interno delle cellule nervose, causandone la morte. Le fasi di blocco, che sappiamo essere essenziali per la formazione di placche amiloidi, impediscono anche la formazione di grovigli, confermando il ruolo dell'amiloide nell'avvio del processo.
La versione della tau presente nei grovigli è caratterizzata dalla presenza di molecole di fosfato in eccesso, e quando il gruppo ha analizzato i possibili modi per bloccare la produzione di tau, ha scoperto che inibendo l'azione di un enzima chiamato GSK3-beta (che fosforila la tau nei neuroni umani) si impedisce la formazione di aggregati tau e dei grovigli, anche in presenza di amiloide-beta abbondante e di placche amiloidi.
"Questo nuovo sistema - che può essere adattato ad altre patologie neurodegenerative - dovrebbe rivoluzionare la scoperta di farmaci, in termini di velocità, costi e rilevanza fisiologica alla malattia", spiega Tanzi. "Provare i farmaci in modelli di topo che in genere hanno depositi cerebrali solo di placche o solo di grovigli, ma non di entrambi, richiede più di un anno ed è molto costoso. Con il nostro modello tridimensionale che riassume sia placche che grovigli, ora possiamo selezionare centinaia di migliaia di farmaci in pochi mesi senza uso di animali, in un sistema che è molto più rilevante per gli eventi che si verificano nel cervello dei malati di Alzheimer".
Fonte: Massachusetts General Hospital via EurekAlert! (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Se Hoon Choi, Young Hye Kim, Matthias Hebisch, Christopher Sliwinski, Seungkyu Lee, Carla D’Avanzo, Hechao Chen, Basavaraj Hooli, Caroline Asselin, Julien Muffat, Justin B. Klee, Can Zhang, Brian J. Wainger, Michael Peitz, Dora M. Kovacs, Clifford J. Woolf, Steven L. Wagner, Rudolph E. Tanzi, Doo Yeon Kim. A three-dimensional human neural cell culture model of Alzheimer’s disease. Nature, 2014; DOI: 10.1038/nature13800
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer onlus di Riese Pio X. I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.
| Sostieni l'Associazione; una donazione, anche minima, ci aiuterà ad assistere malati e famiglie e continuare ad informarti. Clicca qui a destra: |






 Associazione Alzheimer OdV
Associazione Alzheimer OdV