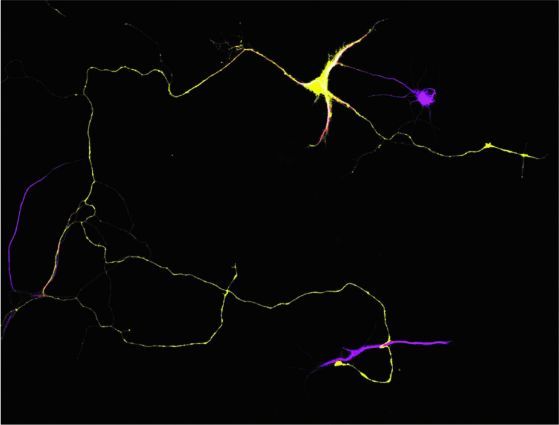
 Neurone ippocampale di topo che esprime una proteina fluorescente verde (GFP, giallo) che crea contatti sinaptici con altri neuroni in colture colorate per la proteina associata ai microtubuli 2B (MAP2B, magenta).
Neurone ippocampale di topo che esprime una proteina fluorescente verde (GFP, giallo) che crea contatti sinaptici con altri neuroni in colture colorate per la proteina associata ai microtubuli 2B (MAP2B, magenta).
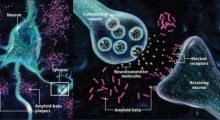
I ricercatori della Tufts University hanno scoperto un meccanismo molecolare che provoca un 'ingorgo' di enzimi che viaggiano su e giù per gli assoni neuronali, provocando l'accumulo di amiloide-beta (Aβ) - una caratteristica fondamentale e causa del morbo di Alzheimer (MA). L'enzima (BACE1) viene integrato, provocando l'intasamento e il rigonfiamento degli assoni a causa dell'aumento della produzione della proteina amiloide tossica.
Lo studio, pubblicato su Science Translational Medicine, riferisce che una mutazione umana, più frequente nei pazienti afro-americani con MA a insorgenza tardiva, innesca un ingorgo di BACE1 negli assoni. Aver identificato questa mutazione è un passo fondamentale per capire i meccanismi molecolari alla base della malattia e fornire una possibile strategia per la diagnosi precoce e trattamenti mirati.
“Negli individui con MA, la comparsa dei sintomi avviene circa 20 anni dopo l'inizio dei primi cambiamenti nel cervello, rendendo l'intervento terapeutico estremamente difficile”, ha detto Giuseppina Tesco, prof.ssa di neuroscienze della Tufts University e autrice senior dello studio. “Perciò abbiamo voluto identificare i meccanismi che portano al rigonfiamento degli assoni durante la fase pre-sintomatica di MA, che potrebbe a sua volta fornire un modo per rilevare presto la malattia e, forse, trattarla in modo più efficace".
I ricercatori della Tufts in precedenza avevano identificato un gene (Gga3) che aiuta a regolare il traffico lungo l'assone del BACE1 (beta-site APP-cleaving enzime 1). Nel nuovo studio, i ricercatori hanno scoperto che quando il gene Gga3 è mutato o mancante nei topi, il loro cervello presenta lo stesso ingorgo distintivo del BACE1 negli assoni rigonfi che si trovano nel cervello post-mortem di pazienti nelle fasi iniziali del MA.
I ricercatori hanno scoperto che rompendo il gene Gga3, si rallenta o si arresta il traffico del BACE1 e di altre proteine lungo l'assone. Essi hanno inoltre rilevato che un Gga3 mutato o mancante porta ad un grave accumulo di BACE1 nell'assone, che si traduce in gonfiore assonale sia nei neuroni in coltura che in un topo modello del MA, prima della deposizione di amiloide.
In diversi studi clinici, gli inibitori BACE somministrati a pazienti con malattia avanzata, che avevano già un notevole accumulo di Aβ e danno neuronale, non hanno avuto successo. I ricercatori si sono chiesti se l'applicazione degli inibitori nelle primissime fasi della malattia potrebbe essere più efficace.
Essi hanno scoperto che gli inibitori impediscono il rigonfiamento degli assoni nei topi e inoltre migliorano il flusso bidirezionale di BACE1. I loro risultati suggeriscono che l'applicazione più precoce degli inibitori BACE1 potrebbe essere più efficace nel rallentare l'accumulo di proteina Aβ.
Utilizzando i dati del National Institute of Mental Health e dell'Alzheimer's Disease Neuroimaging Initiative, i ricercatori hanno scoperto che le mutazioni in Gga3 erano più comuni tra gli afro-americani con diagnosi di MA, rispetto ad altre popolazioni. Anche se la dimensione del campione era piccolo, i ricercatori ritengono che questa scoperta potrebbe aiutare a individuare gli interventi e i trattamenti per la fase iniziale, per questo gruppo di pazienti.
“Il nostro studio fornisce una possibile spiegazione molecolare della prevalenza di assonopatia durante le prime fasi del MA, prima della formazione delle placche amiloidi”, ha detto la Tesco. “La mutazione ha permesso di determinare che le alterazioni assonali possono essere causate dall'accumulo di BACE1. Ora, una zona su cui concentrarsi potrebbe essere l'inibizione del BACE1 per evitare danni assonali precoci e forse questo potrebbe anche rallentare lo sviluppo delle placche amiloidi che portano alla malattia“.
I ricercatori notano che la presenza di 'neurofilamento a catena leggera' (NFL) nel plasma sanguigno è un marcatore del danno assonale, e può essere usato per identificare il momento migliore per usare gli inibitori BACE per prevenire o rallentare la progressione del MA nelle prime fasi pre-sintomatiche.
Fonte: Tufts University (> English) - Traduzione di Franco Pellizzari.
Riferimenti: Selene Lomoio, Rachel Willen, WonHee Kim, Kevin Ho, Edward Robinson, Dmitry Prokopenko, Matthew Kennedy, Rudolph Tanzi, Giuseppina Tesco. Gga3 deletion and a GGA3 rare variant associated with late onset Alzheimer’s disease trigger BACE1 accumulation in axonal swellings. Science Translational Medicine, 18 Nov 2020, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.
bac




 Associazione Alzheimer OdV
Associazione Alzheimer OdV