Attraverso un nuovo modello di topo che imita lo sviluppo dell'Alzheimer negli esseri umani, i ricercatori della Johns Hopkins dicono di essere riusciti a determinare che, per provocare la demenza segno distintivo della malattia, deve avvenire un uno-due di "insulti" biologici gravi nel cervello.
Una descrizione dei loro esperimenti è stata pubblicata online sulla rivista Nature Communications.
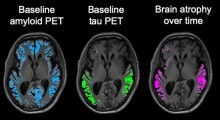
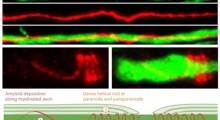
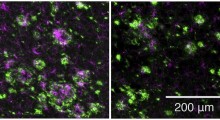
Da decenni sappiamo che l'Alzheimer, la causa più comune di demenza, è associato all'accumulo dei cosiddetti grovigli neurofibrillari (costituiti da ciuffi anormali della proteina tau all'interno delle cellule nervose del cervello), e dalle placche neuritiche (depositi di proteina amiloide-beta fuori di queste cellule) che accompagnano la morte delle cellule nervose nel tessuto cerebrale.
Nell'Alzheimer la tau si raggruppa all'interno delle cellule nervose e l'amiloide-beta lo fa fuori di queste cellule, danneggiando le cellule nervose che controllano la memoria, osserva Philip C. Wong PhD, professore di patologia alla Johns Hopkins University.
Ciò che non era ancora chiaro è il rapporto e la tempistica tra questi due processi di aggregazione, dato che uno avviene all'interno delle cellule e uno fuori dalle cellule, dice il primo e corrispondente autore dello studio Tong Li PhD, assistente professore di patologia alla Johns Hopkins. Studi precedenti sull'Alzheimer ad esordio precoce avevano suggerito che l'accumulo anomalo di amiloide-beta nel cervello inneschi in qualche modo l'aggregazione della tau, portando direttamente alla demenza e alla degenerazione cellulare nel cervello.
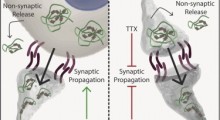
Ma la nuova ricerca da Li, Wong e colleghi suggerisce che l'accumulo di amiloide-beta in sé e per sé è insufficiente per innescare la conversione della tau dallo stato normale a quello anomalo. Al contrario gli studi dimostrano che può innescare una catena di eventi di segnalazione chimica che portano alla "conversione" della tau ad uno stato di aggregazione e al successivo sviluppo dei sintomi.
"Per la prima volta pensiamo di aver capito che l'accumulo di placca amiloide da solo può danneggiare il cervello, ma che in realtà non è sufficiente per guidare la perdita di cellule nervose o i cambiamenti comportamentali e cognitivi", dice Wong. "Sembra essere necessario pure un secondo insulto: la conversione della tau".
Negli esseri umani, il ritardo tra lo sviluppo delle placche di amiloide-beta e i grovigli tau all'interno delle cellule nervose del cervello può essere da 10 a 15 anni o più, dice Li, ma poiché la vita di un topo è solo di 2/3 anni, i modelli animali attuali, che imitano con successo la comparsa di placche di amiloide-beta, non ci danno abbastanza tempo per osservare i cambiamenti nella tau.
Per affrontare questo problema, i ricercatori della Johns Hopkins hanno prodotto geneticamente un modello di topo che usa un frammento di tau per promuovere l'aggregazione di proteina tau normale. Hanno poi incrociato questi topi con altri progettati per accumulare amiloide-beta. Il risultato è un modello di topo che sviluppa la demenza in modo più simile a quanto avviene negli esseri umani, secondo Li.
Durante le dissezioni cerebrali degli animali, i ricercatori hanno scoperto che
- la presenza di placche di amiloide-beta da sole non era sufficiente a provocare la conversione biochimica della tau;
- il dominio di ripetizione della tau (la parte di proteina tau che è responsabile della conversione della tau da normale ad anormale) da solo era insufficiente per la conversione della tau;
- le placche di amiloide-beta devono essere presenti nel cervello per la conversione della tau;
- frammenti di tau potrebbero "seminare" la conversione patologica della tau dipendente dalla placca.
Una conseguenza della nuova ricerca, dice Wong, è che forse può spiegare perché alcuni farmaci progettati per attaccare la malattia dopo la conversione della tau non hanno funzionato: "Il tempo potrebbe essere finito. Se si dovesse intervenire nel periodo di tempo prima della conversione della tau, si potrebbe avere una buona possibilità di migliorare i deficit, la perdita di cellule cerebrali e le conseguenze della malattia".
Il lavoro suggerisce anche che una terapia combinata, progettata per impedire sia la formazione di placche di amiloide-beta, che la conversione patologica della proteina tau, può dare benefici ottimali per la malattia, secondo i ricercatori. Il loro modello di topo potrebbe essere usato per testare nuove terapie.
Fonte: Johns Hopkins Medicine via EurekAlert! (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Tong Li, Kerstin E. Braunstein, Juhong Zhang, Ashley Lau, Leslie Sibener, Christopher Deeble, Philip C. Wong. The neuritic plaque facilitates pathological conversion of tau in an Alzheimer’s disease mouse model. Nature Communications, 2016; 7: 12082 DOI: 10.1038/ncomms12082
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer onlus di Riese Pio X. I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.


 Associazione Alzheimer OdV
Associazione Alzheimer OdV