Ricercatori del Jackson Laboratory elaborano la prima classifica completa del ruolo relativo e del significato di ogni gene e di ogni proteina coinvolti nello sviluppo dell'Alzheimer.
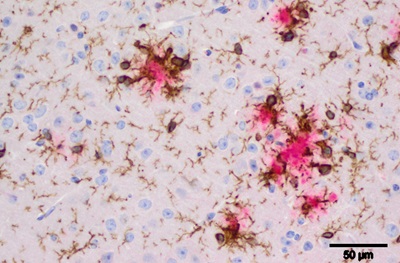
Studiando il genoma umano, analizzando come le proteine sono codificate, o monitorando l'espressione dell'RNA, i ricercatori stanno comprendendo rapidamente e molto meglio i meccanismi genetici e cellulari complessi che sono alla base della demenza.
Ma c'è un problema: mentre le nuove tecnologie stanno rivelando una miriade di strade per la ricerca sul morbo di Alzheimer (MA), è impossibile sapere in anticipo quali percorsi di ricerca porteranno a trattamenti efficaci.
"Abbiamo innumerevoli potenziali obiettivi, ma non sappiamo quali puntare", ha affermato Greg Carter, docente del Jackson Laboratory (JAX), che ha guidato lo studio. "Lo sviluppo dei farmaci è lento e costoso, quindi per approfittare di queste nuove intuizioni, abbiamo bisogno di un modo per dare la priorità in modo efficace".
Ora, Carter e i suoi colleghi dello JAX - in collaborazione con partner di Stanford University, Emory University e Sage Bionetworks - hanno fatto proprio questo, offrendo la prima classifica completa del ruolo e del significato relativo di ogni gene e proteina nello sviluppo della malattia. Il lavoro è stato riferito su Alzheimer & Dementia in occasione della Conferenza Internazionale 2024 dell'Alzheimer's Association del 28 luglio.
"Questo è lo studio più completo eseguito fino ad oggi del cervello dei pazienti di MA", ha detto Carter. "Stiamo integrando la ricerca da più campi, come genetica e -omica, per tutta la durata della vita del paziente e su una scala molto più ampia di quanto era possibile fare finora".
Il team ha impiegato l'apprendimento automatico per mettere insieme e sovrapporre i risultati di oltre due dozzine di studi genetici su larga scala, insieme ad analisi multi-omiche di quasi 2.900 cervelli, per identificare migliaia di potenziali obiettivi per interventi terapeutici. Gli obiettivi sono stati quindi ordinati in 19 'biodomini' separati che riflettono meccanismi biologici che si ritiene contribuiscano al MA.
Carter e i suoi colleghi non volevano solo una lunga lista di bersagli genici e proteici indifferenziati. Invece, ogni bersaglio è associato a una specifica ipotesi terapeutica, rendendo più facile capire come funziona e identificare i candidati alla convalida sperimentale. Il team è riuscito anche a contrassegnare gli obiettivi che potrebbero avere un ruolo nelle prime fasi del MA, supportando lo sviluppo di nuovi strumenti diagnostici e terapeutici per gli interventi pre-sintomatici.
"Questo è incredibilmente importante, ma anche molto impegnativo: la maggior parte dei nostri dati proviene da cervelli post mortem, quindi il nostro lavoro è stato come cercare di dedurre dove è iniziato un incendio forestale dopo che tutto è in cenere", ha affermato Carter. "La nostra modellazione al computer riavvolge efficacemente la progressione della malattia per identificare i primi marcatori che corrispondono alla patologia di fase avanzata".
Tale approccio sta già dando importanti informazioni, tra cui nuove prove che i mitocondri - le centrali energetiche delle cellule - potrebbero avere un ruolo significativo nelle prime fasi del MA. Il team ha trovato una serie di obiettivi promettenti in questo biodominio, suggerendo che la funzione mitocondriale potrebbe essere un indicatore precoce molto forte di MA e un fattore chiave della progressione della malattia.
I risultati e i loro dati completi sono disponibili al pubblico attraverso l'Emory-Sage-SGC-JAX TREAT-AD Center, che fa parte di un consorzio finanziato dai NIH dedicato alla ricerca di MA, offrendo a ricercatori e innovatori di biotecnologie uno strumento fondamentale per supportare ricerche future più intelligenti e più mirate.
"Stiamo adottando un approccio aggressivamente aperto", ha detto Carter. "Se una società biotecnologica o farmaceutica vuole coglierlo e usarlo, può farlo, e speriamo che lo faccia".
Fonte: Jackson Laboratory (> English) - Traduzione di Franco Pellizzari.
Riferimenti: GA Cary, [+11], GW Carter. Genetic and multi‐omic risk assessment of Alzheimer's disease implicates core associated biological domains. Alz&Dem: Transl Res&Clin Interv, 2024, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.



 Associazione Alzheimer OdV
Associazione Alzheimer OdV