Capire come funzionano degli acidi grassi dietetici essenziali può portare a trattamenti efficaci per malattie e condizioni quali ictus, Alzheimer, degenerazione maculare da età, Parkinson e altre malattie retiniche e neurodegenerative. La chiave è essere in grado di intervenire durante le prime fasi della malattia.
Questa è la conclusione di una mini-revisione di Nicolas Bazan MD/PhD, Professore e Direttore, e di Aram Asatryan PhD, ricercatore postdottorato del Centro Neuroscienze alla Louisiana State University di New Orleans, pubblicato sul Journal of Biological Chemistry. La ricerca è disponibile online.
L'acido docosaesaenoico (DHA), un fattore essenziale cruciale dell'Omega-3, produce molecole di segnalazione chiamate «docosanoidi» in risposta ai disordini nello stato di equilibrio all'interno delle cellule, causati da lesioni o malattie. La «neuroprotettina D1» (NDP1) è un docosanoide che ha scoperto il laboratorio di Bazan e della quale ha provato la capacità di proteggere i neuroni, controllando quali geni, e come, rispondono nella retina e nel cervello,.
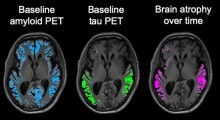
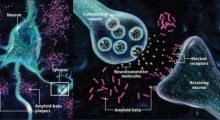
La ricerca mostra che gli eventi preclinici nell'Alzheimer, inclusa la neuroinfiammazione, il danneggiamento delle spine dendritiche (le piccole protrusioni a forma di pomello che aiutano a trasmettere segnali elettrici alla cellula), e i problemi con la comunicazione tra le cellule, corrispondono a un minore contenuto di DHA nel cervello.
La bioattività neuroprotettiva del NPD1 comprende proprietà di modulazione dell'infiammazione, come pure caratteristiche che promuovono la sopravvivenza cellulare, che contribuiscono a ripristinare un equilibrio stabile (omeostasi) all'interno della cellula.
Nei modelli sperimentali di ictus, i ricercatori del Centro Neuroscienze della LSU, guidati da Bazan, hanno dimostrato che la somministrazione di NPD1 riduce la dimensione del danno da ictus e consente anche di salvare il tessuto nel bordo attorno al nucleo dell'ictus, che rimane attivo per un breve periodo di tempo.
La ricerca ha dimostrato anche che il DHA del fegato è mantenuto e concentrato in cellule fotorecettrici e che la degenerazione retinica avviene quando le cellule fotorecettrici non riescono a catturare il DHA. Quando un gene che regola l'assorbimento del DHA è spento, le cellule fotorecettrici muoiono e una singola mutazione di aminoacidi in questo recettore può causare la «retinite pigmentosa».
Le cellule muoiono attraverso vari meccanismi. Tra i responsabili ci può essere una famiglia di specie di ossigeno reattivo, composti formati continuamente come sottoprodotti del metabolismo aerobico come le reazioni ai farmaci e le tossine ambientali o quando i livelli di antiossidanti diminuiscono creando stress ossidativo, nonché l'infiammazione e il processo di malattia. La morte cellulare è considerata reversibile finché non viene passato un primo "punto di non ritorno". Gli autori descrivono il modo in cui l'NPD1 agisce per impedire alle cellule di passare quel punto di non ritorno nei percorsi di attivazione della morte cellulare, che comprendono apoptosi, necrosi, necroptosi, piroptosi e pironecrosi.
La mini-revisione riassume gli effetti del DHA, membro essenziale della famiglia di acidi grassi, e del suo derivato bioattivo NPD1 nel contesto di un obiettivo specifico di regolazione genetica. Gli autori descrivono anche il meccanismo di un percorso di regolazione di un lipido bioattivo che ha un impatto significativo sull'omeostasi cellulare: come l'NPD1 attiva i geni della sopravvivenza e sopprime i geni della morte.
"La complessità organizzativa e funzionale del cervello solleva nuove domande sul modo in cui gli eventi cellulari qui descritti funzionano in risposta a disturbi dell'omeostasi per raggiungere la neuroprotezione in condizioni patologiche", osserva Bazan. "La nostra speranza è che questa conoscenza possa contribuire alla gestione delle fasi iniziali di malattie devastanti come l'Alzheimer, l'ictus, la lesione cerebrale traumatica, la degenerazione maculare legata all'età, il Parkinson e altri".
Fonte: Louisiana State University (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Aram Asatryan and Nicolas G. Bazan. Molecular mechanisms of signaling via the docosanoid neuroprotectin D1 for cellular homeostasis and neuroprotection. Journal of Biological Chemistry, 14/6/2017 doi: 10.1074/jbc.R117.783076
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.




 Associazione Alzheimer OdV
Associazione Alzheimer OdV