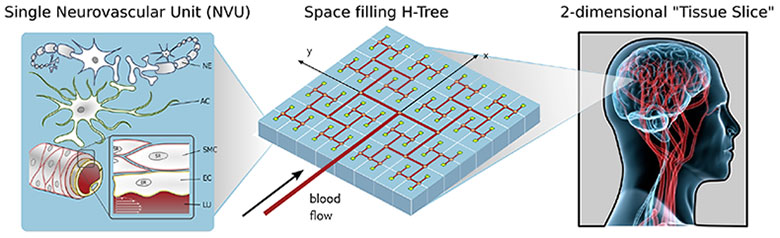
 La figura mostra uno schizzo del gruppo neurovascolare (NVU a sinistra), un blocco di tessuto con albero vascolare incorporato (al centro) e uno schizzo della fetta del tessuto posizionato nella corteccia cerebrale (a destra).
La figura mostra uno schizzo del gruppo neurovascolare (NVU a sinistra), un blocco di tessuto con albero vascolare incorporato (al centro) e uno schizzo della fetta del tessuto posizionato nella corteccia cerebrale (a destra).
Il gruppo di ricerca BRATS della Università di Canterbury sta iniziando delle indagini sulle dinamiche del calcio nel cervello per capire se la mancanza di regolamentazione del flusso sanguigno locale è un precursore dell'Alzheimer.
Il cervello ha un meccanismo specifico che garantisce una fornitura sufficiente e continua di sostanze nutritive a fronte dei cambiamenti locali nella richiesta e nelle condizioni fisiologiche.
L'«accoppiamento neurovascolare» è la capacità di aumentare il flusso di sangue (e quindi la fornitura di ossigeno e glucosio) ai neuroni quando diventano più attivi. In prevalenza esso avviene collegando i neuroni alle cellule muscolari ben amalgamate che circondano i vasi sanguigni, tramite gli astrociti (cellule a forma di stella che collegano i neuroni con i vasi sanguigni).
La prevalenza dell'Alzheimer aumenta in modo esponenziale con l'invecchiamento della popolazione mondiale, oltre il 15% degli over-65 sperimentano un deterioramento cognitivo, e quasi la metà degli over-85 ha una demenza. La sopravvivenza neuronale dipende in modo cruciale dall'accoppiamento neurovascolare e la disfunzione vascolare è un fattore critico per la fisiopatologia dell'Alzheimer.
L'obiettivo dello studio è fornire un modello quantitativo della fornitura regolata di sangue con le cellule collegate in tutto il cervello, che comprende le dinamiche complesse del calcio nei neuroni e negli astrociti.
I ricercatori intendono studiare l'effetto che il calcio ha sulla funzione neuronale e come è disturbato dal suo equilibrio non patologico. In particolare si concentreranno sulla simulazione del ruolo del canale ionico TRPV4 mediato dal calcio, che ha dimostrato di essere potenziato nella concentrazione dell'amiloide-beta e di contribuire ai danni ippocampali.
Il progetto sarà supervisionato dal professor Tim David (University of Canterbury HPC) e comprende la studentessa di dottorato Katharina Dormanns. E' finanziato da un progetto della Canterbury Medical Research Foundation e include il calcolo ad alte prestazioni con la power7 dell'UC HPC.
Il risultato di questa ricerca consentirà di acquisire nuove informazioni sulle anomalie fisiopatologiche che precedono in modo significativo i sintomi clinici evidenti [dell'Alzheimer]. Questo può offrire nuovi bersagli terapeutici associati al sistema vascolare, fornendo al tempo stesso un biomarcatore fisiologico non invasivo che può essere monitorato e consentire un intervento terapeutico pre-clinico.
Fonte: Katharina Dormanns in University of Canterbury (> English text) - Traduzione di Franco Pellizzari.
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer onlus di Riese Pio X. I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.







 Associazione Alzheimer OdV
Associazione Alzheimer OdV