 I ricercatori dell'Università McGill di Montreal hanno scoperto un meccanismo cellulare nell'Alzheimer che può contribuire alla rottura della comunicazione tra i neuroni.
I ricercatori dell'Università McGill di Montreal hanno scoperto un meccanismo cellulare nell'Alzheimer che può contribuire alla rottura della comunicazione tra i neuroni.
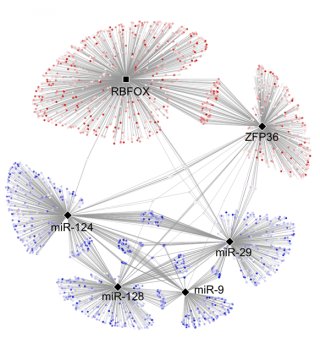
Il loro studio, pubblicato in Nature Communications, fa luce sul ruolo delle molecole di RNA coinvolte nella trasmissione sinaptica, il processo attraverso il quale i neuroni comunicano tra loro.
La scoperta è che, nel tessuto cerebrale dei pazienti di Alzheimer, l'RNA che codifica le proteine sinaptiche è degradato più rapidamente che nelle cellule cerebrali sane.
Hanno anche chiarito che una proteina che aiuta a stabilizzare questo RNA era meno abbondante nei neuroni dei pazienti di Alzheimer.
"Considerati nell'insieme, questi risultati indicano che i livelli insufficienti della proteina RBFOX1, possono contribuire al difetto nei collegamenti, che è un segno distintivo dell'Alzheimer", dice Hamed S. Najafabadi, autore senior della ricerca e assistente professore nel Dipartimento di Genetica Umana della McGill.
Un nuovo pezzo del puzzle
Anche se l'Alzheimer è di gran lunga la forma più comune di demenza, i meccanismi sottostanti non sono ancora del tutto chiari e attualmente non esistono trattamenti per fermare la sua progressione. Lo studio della McGill rivela un nuovo pezzo del puzzle, che potrebbe essere un filone per nuovi approcci terapeutici.
Le cellule umane producono migliaia di tipi diversi di RNA per trasportare informazioni genetiche. Anche l'RNA decade costantemente e l'equilibrio tra produzione e degradazione determina la quantità di un determinato RNA presente nella cellula. Tuttavia gli scienziati sanno relativamente poco su come è controllato il decadimento dell'RNA, in gran parte perché i metodi di misurazione del degrado sono costosi e non applicabili ai tessuti umani.
La ricerca precedente di Najafabadi aveva dimostrato che il degrado del RNA è coinvolto in diverse malattie umane. Comunque la maggior parte di questi risultati è venuto dagli studi sui modelli di linee cellulari delle malattie. "Volevamo misurare direttamente il tasso di degrado dell'RNA nei tessuti umani, ma i metodi disponibili non erano in grado di farlo", spiega Najafabadi. Così il suo team ha trovato un modo per aggirare quel problema. "Abbiamo capito che modellando il processo di produzione e decadimento dell'RNA, possiamo definire un metodo matematico per calcolare il degrado del RNA usando le tecnologie esistenti di genomica".
Misurare il decadimento dell'RNA
Per testare il loro nuovo approccio, i ricercatori della McGill hanno ottenuto l'aiuto di scienziati dell'Università della California di San Francisco. Il team californiano, guidato da Hani Goodarzi, ha allevato delle cellule in laboratorio e ha misurato il tasso di degrado dell'RNA con un metodo convenzionale. Allo stesso tempo, i ricercatori della McGill hanno stimato il tasso con il loro metodo matematico. I due risultati corrispondevano, convalidando il quadro matematico.
Najafabadi e Rached Alkallas, studente laureato della McGill, hanno quindi applicato il metodo matematico per analizzare i dati pubblici disponibili sui tessuti cerebrali di persone morte da Alzheimer. Essi hanno anche analizzato i tessuti cerebrali di persone che non soffrivano del morbo. Il confronto di questi due gruppi ha rivelato il ritmo rapido di degrado dell'RNA e la scarsa disponibilità di proteine RBFOX1 nei pazienti con Alzheimer.
"C'è ancora molto da sapere sul ruolo del degrado dell'RNA nell'Alzheimer e in altre malattie", dice Najafabadi. "Per esempio, perché c'è un calo di RBFOX1 nella malattia? La quantità ridotta di questa proteina è un fattore di rischio, o una caratteristica delle fasi successive della malattia? E possiamo ripristinare almeno una parte della normale funzione dei neuroni controllando l'attività di RBFOX1?"
Fonte: Chris Chipello in McGill University (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Rached Alkallas, Lisa Fish, Hani Goodarzi, Hamed S. Najafabadi. Inference of RNA decay rate from transcriptional profiling highlights the regulatory programs of Alzheimer’s disease. Nature Communications, 2017; 8 (1) DOI: 10.1038/s41467-017-00867-z
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali colelgamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.





 Associazione Alzheimer OdV
Associazione Alzheimer OdV