Ora siamo un passo più vicino ad avere un farmaco che può curare la demenza e la perdita di memoria.
Un gruppo di ricerca in Corea ha scoperto che gli astrociti reattivi, che sono di solito presenti nei pazienti di Alzheimer, producono in modo aberrante ed abbondante il neurotrasmettitore inibitorio primario GABA e lo rilasciano attraverso il canale Best1.
Il GABA rilasciato induce con forza i neuroni vicini a compromettere la trasmissione sinaptica, la plasticità e la memoria. Questa scoperta apre un nuovo capitolo nello sviluppo di nuovi farmaci per il trattamento di tali malattie.
Lo studio condotto dal Dr. C. Justin Lee e dal Dr. Daesoo Kim, entrambi del Korea Institute of Science and Technology (KIST), è pubblicato su Nature Medicine dal 29 giugno.
L'Alzheimer, che è la causa più comune di demenza, è fatale e attualmente non esiste una cura; nella malattia, le cellule cerebrali sono danneggiate e distrutte, con conseguente perdita devastante della memoria. È stato riferito che 1 americano over-65 su 8 ha l'Alzheimer. Nel 2011, 7.600 pazienti anziani con demenza hanno perso la strada di casa e sono diventati senzatetto in Corea. Tuttavia, ad oggi, non c'è una chiara comprensione dei meccanismi alla base della demenza nell'Alzheimer. Fino ad ora la morte neuronale è l'unico meccanismo proposto nella letteratura scientifica.
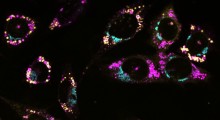
Il team di ricerca ha scoperto che gli astrociti reattivi* nel cervello di topi modello di Alzheimer producono il trasmettitore inibitorio GABA** attraverso l'enzima monoamino ossidasi B*** (MAO-B) e rilasciano GABA attraverso il canale Bestrophin-1 sopprimendo il normale flusso di informazioni durante la trasmissione sinaptica. Sulla base di questa scoperta, il team è riuscito a ridurre la produzione e il rilascio di GABA, inibendo il MAO-B o il Bestrophin-1, migliorando con successo le menomazioni nel firing neuronale [attivazione, emissione di scarica], la trasmissione sinaptica e la memoria nei topi modello di Alzheimer.
Nel test comportamentale, il team ha sfruttato il fatto che i topi tendono a preferire luoghi bui. Se un topo sperimenta una scossa elettrica in un luogo buio, si ricorderà questo evento ed evitarà i luoghi bui da allora in poi. Tuttavia, un topo con l'Alzheimer modellato non può ricordare se tale shock è legato a luoghi oscuri e continua a tornare lì. Il team ha dimostrato che il trattamento di questi topi con un inibitore del MAO-B recupera completamente la loro memoria. La selegilina **** è attualmente usata nel Parkinson come terapia aggiuntiva ed è considerata una delle migliori medicine potenziali per inibire il MAO-B. Ma in precedenza è stato dimostrato che è meno efficace nell'Alzheimer.
Il gruppo ha dimostrato che la selegilina è efficace per un breve tempo, ma quando viene usata nel lungo periodo, perde la sua efficacia nei topi modello di Alzheimer. Se trattati per 1 settimana, la selegilina porta il firing neuronale ad un livello normale. Ma quando sono trattati per 2/4 settimane, il firing neuronale torna ai livelli dei topi non trattati. Da questi risultati, il gruppo ha proposto che c'è la necessità urgente di un nuovo farmaco che abbia effetti di lunga durata.
Il Dr. C. Justin Lee ha detto: "Con questo studio riveliamo il meccanismo innovativo della perdita di memoria dei malati di Alzheimer. Proponiamo anche nuovi bersagli terapeutici, che includono la produzione di GABA e i meccanismi di rilascio negli astrociti reattivi per il trattamento dell'Alzheimer. Inoltre, forniamo un trampolino di lancio per lo sviluppo degli inibitori del MAO-B con efficacia prolungata".
***********
La ricerca è stata condotta al WCI Center for Functional Connectomics, Brain Science Institute del Korea Institute of Science and Technology, in collaborazione con gruppi di ricerca nazionali e internazionali, tra cui il KAIST. Lo studio è stato finanziato dal Ministero Coreano della Scienza ICT e della Pianificazione e dalla Fondazione Nazionale di Ricerca della Corea (NRF) nell'ambito del Progetto World Class Institute e Flagship Project del KIST Brain Science Institute.
Definizioni
* Gli astrociti
Gli astrociti sono il tipo di cellule più abbondante del cervello umano. Essi svolgono molte funzioni, tra cui il supporto biochimico delle cellule endoteliali che formano la barriera emato-encefalica, la fornitura di nutrienti al tessuto nervoso, il mantenimento dell'equilibrio ionico extracellulare e hanno un ruolo nel processo di riparazione e cicatrizzazione del cervello e del midollo spinale dopo una lesione traumatica.
** Acido gamma-aminobutirrico (GABA)
L'acido γ-aminobutirrico o GABA è il principale neurotrasmettitore inibitorio nel sistema nervoso centrale dei mammiferi. Esso ha un ruolo nella regolazione dell'eccitabilità neuronale in tutto il sistema nervoso. Negli esseri umani, il GABA è direttamente responsabile anche della regolazione del tono muscolare.
*** Monoamino ossidasi B (MAOB)
Il monoamino ossidasi B, noto anche come MAOB, è un enzima che nell'uomo è codificato dal gene MAOB. La proteina codificata da questo gene appartenente alla famiglia flavina monoamino ossidasi. Si tratta di un enzima localizzato sulla membrana mitocondriale esterna. Esso catalizza la deaminazione ossidativa delle ammine biogene e xenobiotiche e ha un ruolo importante nel metabolismo delle ammine vasoattive e neuroattive e nel sistema nervoso centrale e nei tessuti periferici.
**** Selegilina
La selegilina è un farmaco usato per il trattamento della fase iniziale di Parkinson, depressione e demenza. In dosi normali cliniche è un inibitore delle MAO-B irreversibile e selettivo.
Fonte: Korea Institute of Science and Technology (KIST) (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Seonmi Jo, Oleg Yarishkin, Yu Jin Hwang, Ye Eun Chun, Mijeong Park, Dong Ho Woo, Jin Young Bae, Taekeun Kim, Jaekwang Lee, Heejung Chun, Hyun Jung Park, Da Yong Lee, Jinpyo Hong, Hye Yun Kim, Soo-Jin Oh, Seung Ju Park, Hyo Lee, Bo-Eun Yoon, YoungSoo Kim, Yong Jeong, Insop Shim, Yong Chul Bae, Jeiwon Cho, Neil W Kowall, Hoon Ryu, Eunmi Hwang, Daesoo Kim, C Justin Lee. GABA from reactive astrocytes impairs memory in mouse models of Alzheimer's disease. Nature Medicine, 2014; DOI: 10.1038/nm.3639
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer onlus di Riese Pio X. I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.
| Sostieni l'Associazione; una donazione, anche minima, ci aiuterà ad assistere malati e famiglie e continuare ad informarti. Clicca qui a destra: |







 Associazione Alzheimer OdV
Associazione Alzheimer OdV