La legatura alogena è applicata da qualche tempo nell'ingegneria dei cristalli, nella ricerca sui materiali e nelle nanotecnologie.
Scienziati dell'Heidelberg Institute for Theoretical Studies (HITS) e dell'Accademia Ceca delle Scienze di Praga hanno ora sviluppato un nuovo strumento da utilizzare nelle legature alogene per applicazioni di scoperte farmacologiche.
La chimica alogena è sfruttata dai chimici di medicinali da quasi 70 anni. Fino ad oggi, gli alogeni erano considerati utili per ottimizzare le cosiddette proprietà ADMET (Assorbimento, Distribuzione, Metabolismo, Escrezione, Tossicità) di potenziali farmaci: migliorano l'assorbimento orale e agevolano l'attraversamento delle barriere biologich; sono utili per il riempimento delle piccole cavità idrofobiche presenti in molte proteine bersaglio; e prolungano la durata del farmaco. In breve: rendono più simili ai farmaci dei composti di interesse. Tuttavia sono molto ignorate nello sviluppo pre-clinico di farmaci le interazioni dirette mediate da atomi di alogeno.
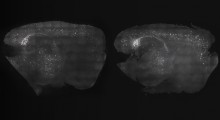
 Figura a sinistra: la distribuzione della carica attorno alla molecola bromobenzene. In blu le regioni di potenziale elettrostatico negativo, in grigio quelle positive. Il disco grigio in prima linea rappresenta il foro sigma. Figura a destra: la sovrapposizione delle posizioni previte di legame dell'inibitore K17 della caseina chinasi 2 (codice PDB 2OXY) con (rosso) e senza (blu) fori sigma espliciti (ESH) e confronto con la struttura cristallina (grigio). (Credit: Agnieszka Bronowska / HITS) |
Recentemente, scienziati di Heidelberg e di Praga, che lavorano nella chimica quantistica e nella progettazione di farmaci a base di struttura, hanno messo a punto un nuovo strumento usare le legatura alogena nella chimica farmaceutica computazionale e nelle applicazioni per la scoperta di farmaci. Lo studio, condotto dalla Dr. Agnieszka Bronowska dell'Istituto per gli Studi Teorici di Heidelberg (HITS), in collaborazione con gli scienziati dell'Accademia Ceca delle Scienze, è stato pubblicato nella rivista Chemical Communication.
La maggior parte degli alogeni - tranne il fluoro - hanno proprietà uniche che permettono loro di stabilizzare l'interazione diretta tra farmaci potenziali e le loro proteine obiettivo. Queste proprietà sono di origine chimica quantistica; in particolare l'anisotropia della distribuzione di carica attorno all'atomo di alogeno, quando è legato a un substrato che attrae l'elettrone.
Pur essendo carichi negativamente, gli alogeni hanno regioni che rimangono cariche positivamente (figura a sinistra nell'immagine qui sopra). Queste regioni, chiamati fori sigma, sono responsabili del carattere direzionale e stabilizzante della legatura alogena con altri atomi elettronegativi, come l'ossigeno o l'azoto. Trascurare i fori sigma porta a fare errori nella previsione della struttura e nell'energetica di complessi proteici per medicinali e quindi al fallimento nello sviluppo di farmaci.
Approssimando i fori sigma a carica positiva con un pseudo-atomo carico e privo di massa (chiamato foro sigma esplicito o ESH), Agnieszka Bronowska e i suoi colleghi hanno incorporato un effetto chimico quantistico nei metodi di calcolo più veloci (e molto meno precisi), applicabili alla progettazione di farmaci basata sulle strutture. "Abbiamo testato quasi un centinaio di complessi tra proteine rilevanti in medicina e molecole alogenate", dice la Bronowska. "I risultati mostrano un miglioramento significativo nella descrizione di tali complessi a seguito dell'introduzione di ESH".
Il nuovo metodo è già utilizzato da gruppi di ricerca nella Repubblica Ceca, nel Regno Unito e negli Stati Uniti per la progettazione di nuovi composti per il trattamento di tumori resistenti alla chemioterapia, di malattie infettive, e dell'Alzheimer.
***********************
Cosa pensi di questo articolo? Ti è stato utile? Hai rilievi, riserve, integrazioni? Conosci casi o ti è successo qualcosa che lo conferma? o lo smentisce? Puoi usare il modulo dei commenti qui sotto per dire la tua opinione. Che è importante e unica.
***********************
Fonte: Materiale dell'Heidelberg Institute for Theoretical Studies.
Riferimento: Michal Kolář, Pavel Hobza, Agnieszka K. Bronowska. Plugging the explicit σ-holes in molecular docking. Chemical Communications, 2013; 49 (10): 981 DOI: 10.1039/C2CC37584B.
Pubblicato in ScienceDaily il 19 Gennaio 2013 - Traduzione di Franco Pellizzari.
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer onlus di Riese Pio X. I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari proposti da Google sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.
| Sostieni l'Associazione; una donazione, anche minima, ci aiuterà ad assistere malati e famiglie e continuare ad informarti. Clicca qui a destra: |





 Associazione Alzheimer OdV
Associazione Alzheimer OdV