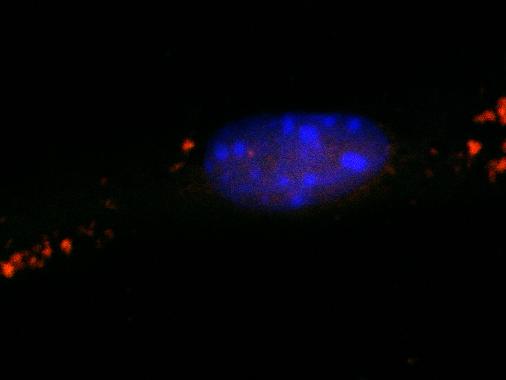
 Cellule nervose sane di controllo con 'sacchetti della spazzatura' (rosso) intatti. (Fonte: © AG van Echten-Deckert/Uni Bonn)Uno studio guidato dall'Università di Bonn apre una nuova prospettiva per quanto riguarda lo sviluppo della demenza.
Cellule nervose sane di controllo con 'sacchetti della spazzatura' (rosso) intatti. (Fonte: © AG van Echten-Deckert/Uni Bonn)Uno studio guidato dall'Università di Bonn apre una nuova prospettiva per quanto riguarda lo sviluppo della demenza.
Gli scienziati hanno bloccato il degrado di una certa molecola di grasso nel cervello di topi e la conseguenza è stata che gli animali hanno mostrato problemi di apprendimento e di memoria, come pure un aumento significativo della quantità di proteine specifiche di Alzheimer nel loro cervello.
I ricercatori ora hanno un indizio sul perché i topi diventano ottusi. I risultati sono pubblicati nella rivista scientifica Autophagy.
Oltre all'acqua, il nostro cervello è ricco di lipidi, in parole semplici, grassi. I lipidi agiscono, ad esempio, come strato isolante attorno alle fibre nervose e pertanto impediscono i cortocircuiti. Tuttavia, essi sono anche uno dei componenti principali delle delicate membrane che circondano le cellule del cervello.
Gli sfingolipidi, un tipo speciale di lipidi, sono molto arricchiti nel cervello. Uno dei loro prodotti di degradazione, l'S1P, può avere un ruolo centrale nello sviluppo dell'Alzheimer e di altre forme di demenza. "Abbiamo allevato topi incapaci di scindere l'S1P in gran parte del cervello", spiega la dott.ssa Gerhild van Echten-Deckert. "Gli animali hanno quindi mostrato una capacità ridotta di apprendimento e di memoria".
La Van Echten-Deckert fa ricerca all'Istituto LIMES (acronimo di 'Life and Medical Sciences') dell'Università di Bonn come assistente professore. Da molto tempo è uno dei pochi esperti al mondo interessati al ruolo dell'S1P nel cervello. Il nuovo studio potrebbe cambiare tutto questo in maniera fondamentale, dato che le conseguenze a lungo termine dell'incapacità di degradazione dell'S1P sono state dimostrate da ricercatori provenienti dall'Università di Bonn, dall'Ospedale Universitario di Jena, dal Centro tedesco per le malattie neurodegenerative (DZNE) e da San Francisco e Madrid.
L'«auto-mangiarsi» mantiene il cervello sano
Normalmente l'S1P è scisso in prodotti più semplici. Uno dei prodotti generati dalla degradazione è importante per un percorso metabolico vitale, chiamato «autofagia». La parola autofagia (che letteralmente significa 'auto-mangiarsi'), e il percorso relativo, consente alle cellule di digerire e riciclare i propri componenti. Dalle cellule vengono quindi espulse le proteine difettose e gli organi cellulari che non funzionano più correttamente.
L'eliminazione dei rifiuti intracellulari funziona in due fasi: la prima è l'imballo dei rifiuti in piccoli 'sacchetti di spazzatura'. Questi poi si fondono con altri 'sacchetti' che contengono enzimi altamente reattivi. Gli enzimi 'distruggono' il contenuto dei sacchetti di spazzatura e quindi se ne liberano.
Il prodotto di degrado dell'S1P è coinvolto nell'imballaggio dei rifiuti nei sacchetti intracellulari di spazzatura. "Se l'S1P non è degradato, si formano meno sacchetti di rifiuti chiusi e l'autofagia non funziona più accuratamente", spiega il primo autore dello studio Daniel Mitroi, che ha completato di recente il dottorato all'Istituto LIMES. "I materiali nocivi quindi si accumulavano nel cervello dei nostri topi, inclusa la proteina APP, che ha un ruolo chiave nello sviluppo dell'Alzheimer".
Poiché l'autofagia è cruciale per il normale funzionamento del cervello, l'eliminazione impropria dei rifiuti intracellulari provoca gravi malattie. Così l'anno scorso il premio Nobel per la medicina è stato assegnato allo scienziato giapponese Yoshinori Ohsumi per il suo notevole lavoro su questo meccanismo vitale.
I risultati dello studio in corso stanno chiarendo un meccanismo precedentemente trascurato dello sviluppo della demenza. "A lungo termine, il nostro lavoro può contribuire a sviluppare strategie di trattamento efficaci per i disturbi cerebrali", si augura la dott.ssa van Echten-Deckert.
Fonte: University of Bonn via EurekAlert! (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Daniel N. Mitroi, Indulekha Karunakaran, Markus Gräler, Julie D. Saba, Dan Ehninger, María Dolores Ledesma & Gerhild van Echten-Deckert. SGPL1 (sphingosine phosphate lyase 1) modulates neuronal autophagy via phosphatidylethanolamine production. Autophagy, Pages 885-899, Published online: 28 Feb 2017. DOI: 10.1080/15548627.2017.1291471
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer onlus di Riese Pio X. I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.





 Associazione Alzheimer OdV
Associazione Alzheimer OdV