Uno studio recente implica un nuovo colpevole nello sviluppo dell'Alzheimer. La ricerca rivela che la proteina ßCTF - il precursore del peptide amiloide-beta (Aß) - è attiva nelle primissime fasi dell'Alzheimer e fa iniziare una serie di anomalie che comportano la perdita di gruppi di neuroni critici per la formazione della memoria.
Lo studio, condotto al Nathan S. Kline Institute for Psychiatric Research (NKI) e al Langone Medical Center della New York University, è stato pubblicato online ieri, 21 Luglio 2015, sulla rivista Molecular Psychiatry, ed è stato selezionato per la copertina di una prossima edizione.
Le sue scoperte, che coinvolgono la ßCTF, hanno implicazioni significative per le strategie di trattamento e per promuovere lo sviluppo di farmaci di Alzheimer. Attualmente, la strategia più comune per il trattamento dell'Alzheimer punta il peptide amiloide-ß, con un modesto successo negli studi clinici.
I risultati di questa ricerca suggeriscono che i farmaci che possono ridurre i livelli di βCTF, così come quelli dell'amiloide-beta (come la classe di inibitori BACE1 attualmente in fase di sviluppo), possono contribuire a rallentare o arrestare la progressione dell'Alzheimer.
La βCTF si forma durante l'endocitosi, il processo con cui le cellule assorbono nutrienti e campionano vari materiali dall'ambiente esterno. È noto da tempo che nell'Alzheimer si sviluppano molto presto anomalie dell'endocitosi, ben prima dell'apparizione dei sintomi clinici, e che le forme varianti dei geni che controllano l'endocitosi sono citate di frequente come fattori di rischio che promuovono l'Alzheimer.
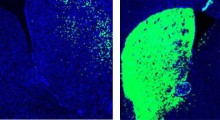
Gli endosomi - le vescicole membranose che mediano l'endocitosi - iniziano a gonfiarsi in modo anomalo in alcuni neuroni, anche nella prima infanzia nella sindrome di Down, una disabilità dello sviluppo che porta quasi sempre all'insorgenza precoce di AD (la ricerca indica che oltre il 75 per cento degli over-65 con sindrome di Down, hanno l'Alzheimer).
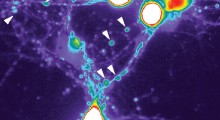
Il gruppo di ricerca NYU Langone/NKI, guidato da Ralph Nixon MD/PhD, professore nei dipartimenti di psichiatria e biologia cellulare della Facoltà di Medicina del NYU Langone e direttore del Centro per la ricerca sulla demenza al Nathan S. Kline Institute for Psychiatric Research, ha scoperto che, nell'Alzheimer e nella sindrome di Down, la βCTF si forma più rapidamente sugli endosomi, innescando un percorso molecolare che porta alla perdita dei neuroni coinvolti nella memoria.
I ricercatori hanno scoperto che l'APPL1, una proteina non correlata alla proteina precursore dell'amiloide (APP), nonostante il suo acronimo simile, lega direttamente la βCTF ad una seconda proteina, Rab5, nota per attivare la catena molecolare di eventi che portano alla neurodegenerazione. L'abbassamento dei livelli di APPL1 nelle cellule di individui con sindrome di Down ha abolito l'endocitosi anomala, indicando il ruolo vitale dell'APPL1 in questa cascata molecolare.
Aver identificato l'APPL1 come anello mancante di una catena ben descritta di eventi associati alla fase molto precoce della patologia di Alzheimer implica un contributo diretto della ßCTF nello sviluppo dell'Alzheimer. In particolare, si ritiene che la recente scoperta di una mutazione dell'APP che abbassa in modo unico, piuttosto che aumentare, il rischio di Alzheimer, agisca rallentando la formazione di ßCTF.
Anche se i risultati attuali non modificano l'importanza dell'Aß come colpevole e bersaglio per una terapia di Alzheimer, essi ora sottolineano l'importanza della ßCTF come fattore chiave per lo sviluppo della malattia. "Sarà importante considerare il ruolo della βCTF nella progettazione di future terapie per l'Alzheimer e nell'interpretazione degli attuali studi clinici di inibitori BACE1. Gli esperimenti su inibitori BACE1 sono stati considerati un test dell'ipotesi Aß/amiloide, ma l'azione primaria di questi inibitori è in realtà il blocco della formazione di ßCTF, il precursore dell'Aß", ha detto Ralph A. Nixon MD/PhD.
Fonte: Nathan Kline Institute for Psychiatric Research via EurekAlert! (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: S Kim, Y Sato, P S Mohan, C Peterhoff, A Pensalfini, A Rigoglioso, Y Jiang, R A Nixon. Evidence that the rab5 effector APPL1 mediates APP-βCTF-induced dysfunction of endosomes in Down syndrome and Alzheimer’s disease. Molecular Psychiatry, 2015; DOI: 10.1038/MP.2015.97
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non dipende da, nè impegna l'Associazione Alzheimer onlus di Riese Pio X. I siti terzi raggiungibili da eventuali links contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.



 Associazione Alzheimer OdV
Associazione Alzheimer OdV