Il numero crescente di casi di morbo di Alzheimer (MA), che si prevede possa raggiungere 135 milioni entro il 2050, sottolinea la necessità urgente di terapie efficaci.
L'evidenza accumulata indica che nei pazienti di MA c'è una compromissione del meccanismo metabolico che parte diversi decenni prima dell'inizio della demenza e del deterioramento della funzione cognitiva. Il metabolismo ridotto deriva da una disfunzione dei mitocondri, che sono responsabili della produzione della maggior parte dell'energia della cellula, ma sono anche coinvolti nella morte cellulare, nell'infiammazione e nella risposta immunitaria.
Nonostante la malattia sia collegata alla disfunzione mitocondriale, attualmente nessun farmaco candidato ha puntato questo aspetto. I ricercatori dell'Università Ben-Gurion del Negev (Israele) stanno proponendo un nuovo approccio terapeutico che punta il guardiano mitocondriale, il 'canale anionico 1 dipendente dal voltaggio' (VDAC1, voltage-dependent anion channel-1), che controlla l'attività mitocondriale e quindi la vita e la morte della cellula.
Il nuovo obiettivo proposto, e la relativa terapia, hanno dimostrato di migliorare significativamente diversi parametri nei topi modello, come riferito su Translational Neurodegeneration alla fine di dicembre.
Il VDAC1 ha un ruolo cruciale nel processo di morte cellulare mediato dai mitocondri, motivo per cui il team di ricercatori guidato dalla prof.ssa Varda Shoshan-Barmatz del National Institute for Biotechnology nel Negev ha scelto di concentrare gli sforzi sulla disfunzione dei mitocondri in topi modello del MA, come bersaglio di trattamento.
La ricerca ha dimostrato che un aumento della quantità della proteina VDAC1 nella cellula porta alla sua organizzazione come un anello, con un grande canale attraverso il quale escono le proteine fattore-di-morte e il DNA mitocondriale, causando rispettivamente la morte cellulare e una risposta immunitaria.
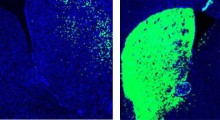
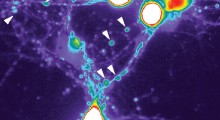
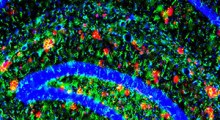
Un aumento notevole dei livelli di VDAC1 è stato riscontrato nelle malattie cardiache, intestinali (Crohn), autoimmuni (lupus) e altre. Qui, i ricercatori mostrano che la proteina è prodotta a livelli enormi nel cervello di topi modello di MA ed è concentrata nelle cellule nervose intorno alla placca, provocando la loro morte.
La prof.ssa Shoshan-Barmatz ha sviluppato una piccola molecola, VBIT-4, che si lega al VDAC1 e impedisce i cambiamenti patofisiologici associati al MA. La VBIT-4, una molecola che può attraversare la barriera emato-encefalica (BBB), è in grado di prevenire i cambiamenti patofisiologici associati al MA, come la morte delle cellule neuronali, la neuroinfiammazione e le disfunzioni neuro-metaboliche.
Inoltre, ha anche indotto un fenotipo neuroprotettivo negli astrociti e nelle microglia, che sono di norma pro-infiammatorie e neurotossiche. Ciò significa non solo che il trattamento ha protetto dalla degenerazione, ma che ha anche promosso la crescita sana e il normale funzionamento dei neuroni. Inoltre, la terapia ha anche impedito il declino delle capacità cognitive, come l'apprendimento e la memoria, nei topi.
È interessante notare che gli effetti protettivi sono stati acquisiti senza ridurre significativamente le placche di tau o amiloide (Aβ), comunemente ritenute come le cause principali del MA. Ciò suggerisce che l'ipotesi cascata-Aβ, secondo la quale questi elementi sono la causa principale della malattia, potrebbe non riflettere accuratamente la causa sottostante della malattia.
"Puntare il VDAC1 con una nuova molecola che abbiamo sviluppato presenta un approccio innovativo al trattamento del MA e può anche essere usato come trattamento preventivo", ha affermato la prof.ssa Shoshan-Barmatz.
Fonte: Ben-Gurion University of the Negev (> English) - Traduzione di Franco Pellizzari.
Riferimenti: A Verma, ...[+11], V Shoshan-Barmatz. Targeting the overexpressed mitochondrial protein VDAC1 in a mouse model of Alzheimer’s disease protects against mitochondrial dysfunction and mitigates brain pathology. Transl Neurodeg, 28 Dec 2022, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.






 Associazione Alzheimer OdV
Associazione Alzheimer OdV