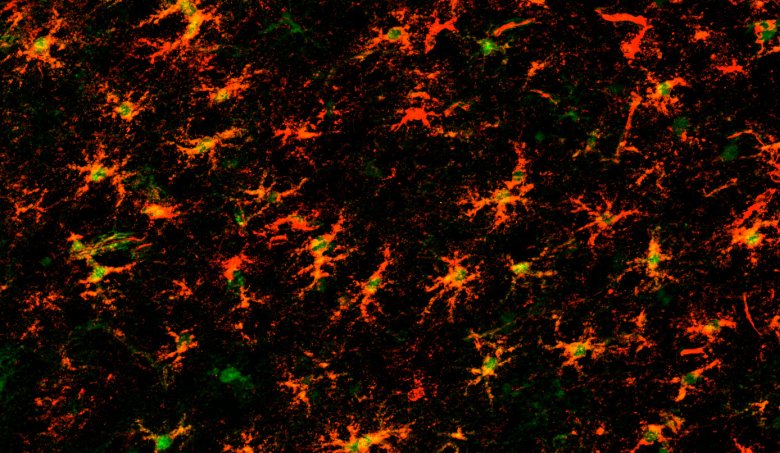
 I ribosomi negli astrociti sono marcati in rosso con il metodo ribo-tag. La macchia verde indica il nucleo delle cellule di supporto a forma di stella (Fonte: Istituto Salk)
I ribosomi negli astrociti sono marcati in rosso con il metodo ribo-tag. La macchia verde indica il nucleo delle cellule di supporto a forma di stella (Fonte: Istituto Salk)
Ricercatori dell'Istituto Salk hanno scoperto che i geni che sono attivi all'inizio dello sviluppo del cervello, per potare le connessioni in eccesso tra i neuroni, sono nuovamente attivati negli astrociti (le cellule di supporto ai neuroni) che invecchiano, spiegando potenzialmente anche perché il cervello sano non funziona bene con l'età.
Il lavoro, apparso il 2 gennaio 2018 su Cell Reports, suggerisce che gli astrociti possono essere buoni bersagli terapeutici per prevenire o invertire gli effetti del normale invecchiamento.
"Gran parte del lavoro per esaminare l'influenza delle cellule cerebrali non neuronali - in particolare gli astrociti - sui neuroni è stata portata avanti nel cervello giovane durante lo sviluppo", dice Nicola Allen, assistente professore nel Laboratorio di Neurobiologia Molecolare del Salk. "Ma volevamo capire perché in un cervello sano che invecchia i neuroni non comunicano più bene come prima".
Sebbene non siano stati studiati così bene come i neuroni, gli astrociti (che derivano il nome dal loro aspetto a forma di stella) costituiscono da un terzo a metà di tutte le cellule del cervello e sono considerati sempre più cruciali per la funzione dei neuroni. La Allen aveva scoperto in precedenza una classe di proteine secrete dagli astrociti che aiutano i neuroni a formare connessioni attive, chiamate sinapsi. Senza questo aiuto, i neuroni non comunicano.
I neuroscienziati sanno che nel cervello neonatale, in fase di sviluppo, le sinapsi vengono attivate e disattivate, mentre nel cervello adulto sono per lo più stabili. Ma nel cervello che invecchia, i neuroni iniziano a perdere connessioni e non comunicano più bene.
La Allen e lo studente laureato Matthew Boisvert si sono chiesti se i cambiamenti delle sinapsi e della comunicazione neuronale durante l'invecchiamento potessero essere correlati ai cambiamenti negli astrociti. Per scoprirlo, il duo ha deciso di confrontare l'espressione genica negli astrociti nel cervello adulto rispetto a quello invecchiato nei topi. Ciò avrebbe potuto dare un'idea di quali geni sono attivi nelle due fasi.
Boisvert ha scelto di confrontare i topi di quattro mesi (la loro età adulta) con quelli di due anni, che sono piuttosto anziani. Ha usato una tecnologia molecolare chiamata 'ribo-tag' che gli ha permesso di scoprire quali geni venivano trasformati in proteine dagli astrociti. Funziona isolando i macchinari cellulari che producono proteine (chiamati ribosomi), che trasformano le copie mRNA del DNA (geni) in proteine. Prendendo una sorta di istantanea molecolare dei ribosomi di un astrocita, è possibile vedere tutte le copie di mRNA in elaborazione e quindi sapere quali geni sono attivi.
Per sviluppare una visione completa dell'espressione genica degli astrociti, la coppia ha usato questa tecnica in quattro aree molto diverse del cervello del topo: due regioni della corteccia, più l'ipotalamo e il cervelletto.
Con loro sorpresa, hanno scoperto che la maggior parte delle proprietà che rendono astrocita un astrocita non cambia molto con l'età; l'espressione genica è abbastanza coerente nel tempo. Ma ecco il cambiamento: i geni che durante lo sviluppo avrebbero normalmente causato la perdita di connessioni tra i neuroni si sono attivati di nuovo negli astrociti anziani.
"Questo suggerisce che c'è una sorta di programma genetico che viene riattivato in questi astrociti mentre invecchiano, causando la perdita di connessioni tra i neuroni", dice Allen.
È interessante notare che le aree in cui gli astrociti sembravano più diversi erano le aree del cervello in cui i neuroni notoriamente funzionano meno bene con l'età o addirittura muoiono: il cervelletto e l'ipotalamo. "Questo può spiegare perché con l'età diminuisce il metabolismo e peggiora la coordinazione, perché queste funzioni sono coordinate dall'ipotalamo e dal cervelletto", aggiunge Boisvert.
Il team ha reso pubblici questi dati dello studio, a disposizione di altri ricercatori. In futuro, il laboratorio intende confrontare gli astrociti che invecchiano con quelli di modelli di malattia per vedere se possono esserci cambiamenti prepatologici che determinano il passaggio alla malattia.
Fonte: Salk Institute (> English text) - Traduzione di Franco Pellizzari.
Riferimenti: Matthew M. Boisvert, Galina A. Erikson, Maxim N. Shokhirev, Nicola J. Allen. The Aging Astrocyte Transcriptome from Multiple Regions of the Mouse Brain. Cell Reports, 2018; 22 (1): 269 DOI: 10.1016/j.celrep.2017.12.039
Copyright: Tutti i diritti di eventuali testi o marchi citati nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer onlus di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali colelgamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.



 Associazione Alzheimer OdV
Associazione Alzheimer OdV