Un team dell'istituto di ricerca Scripps ha ripristinato le connessioni da neurone a neurone nelle cellule umane
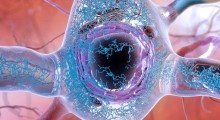
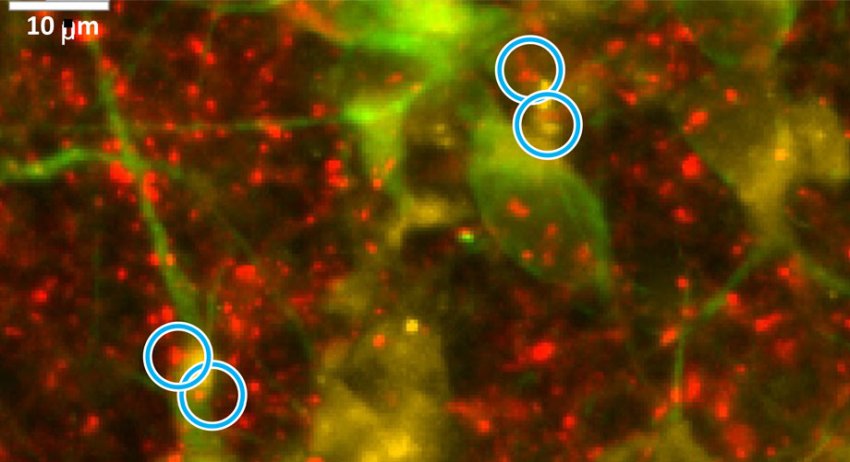 Con l'Alzheimer le cellule nervose mostrano meno connessioni tra loro (sinapsi), qui cerchiate di blu. Metà delle sinapsi sono in rosso e l'altra metà in giallo. (Fonte: Scripps Research)
Con l'Alzheimer le cellule nervose mostrano meno connessioni tra loro (sinapsi), qui cerchiate di blu. Metà delle sinapsi sono in rosso e l'altra metà in giallo. (Fonte: Scripps Research)
Le cellule nervose nel cervello richiedono un'enorme quantità di energia per sopravvivere e mantenere le connessioni che usano per comunicare con altre cellule nervose. Nel morbo di Alzheimer (MA), la capacità di produrre energia è compromessa e le connessioni (chiamate sinapsi) tra le cellule nervose alla fine si separano e appassiscono, causando l'affievolimento e la sparizione dei ricordi.
Un team di ricerca dello Scripps, come riferito su Advanced Science il 18 gennaio 2024, ha ora identificato nelle cellule cerebrali le reazioni energetiche che si guastano e portano alla neurodegenerazione. Usando una piccola molecola per affrontare il malfunzionamento che avviene nei mitocondri, i principali produttori di energia della cellula, i ricercatori hanno mostrato che si sono ripristinate molte connessioni da neurone a neurone nei modelli di cellule nervose derivate dalle cellule staminali di pazienti umani di MA.
Questi risultati evidenziano che il miglioramento del metabolismo mitocondriale potrebbe essere un promettente bersaglio terapeutico per il MA e i disturbi correlati.
"Abbiamo pensato che se riuscissimo a riparare l'attività metabolica nei mitocondri, forse potremmo recuperare la produzione di energia", afferma l'autore senior Stuart Lipton MD/PhD, professore e condirettore del New Medicines Center dello Scripps Risearch e neurologo clinico a La Jolla, in California. "Usando neuroni umani derivati da persone con MA, è stato sufficiente proteggere i livelli di energia per salvare un gran numero di connessioni neuronali".
Nel nuovo studio, Lipton e il suo team hanno trovato un blocco negli enzimi che producono energia a causa di una marcatura anormale di atomi di azoto (N) e ossigeno (O) su un atomo di zolfo, che insieme formano un enzima 'SNO' disfunzionale. Questa reazione è definita S-nitrosilazione e il team ha dimostrato che nei neuroni cerebrali del MA avviene una 'tempesta-SNO' virtuale di queste reazioni.
Lipton e i suoi colleghi inizialmente hanno scoperto il 'marcatoreSNO' sugli enzimi energetici, confrontando cervelli umani (ottenuti all'autopsia di persone con MA) con quelli di persone senza malattia cerebrale. I ricercatori hanno successivamente generato cellule nervose dalle cellule staminali derivate da biopsie cutanee di persone con e senza una mutazione genetica che causa il MA.
Quindi, usando una serie di marcatori metabolici e un apparato di misurazione dell'ossigeno, hanno calcolato la produzione di energia cellulare e hanno identificato deficit unici nelle cellule nervose del MA rispetto ai controlli.
I ricercatori hanno scoperto che i neuroni avevano un ciclo di Krebs interrotto, che è il processo cellulare nei mitocondri che produce la maggior parte della fonte di potenza molecolare cruciale del corpo, l'ATP. Il team ha individuato un collo di bottiglia (o blocco) nella fase in cui si forma una molecola chiave, il succinato, che guida gran parte della successiva produzione di ATP.
Nello studio, il collo di bottiglia ha inibito la capacità dei mitocondri di produrre l'energia necessaria per sostenere i neuroni e le loro numerose connessioni. I ricercatori hanno ipotizzato che, riuscendo a fornire alcune delle molecole di succinato mancanti, si potrebbe ripristinare la produzione di energia, facendo essenzialmente ripartire il ciclo di Krebs mitocondriale bloccato.
Poiché il succinato non viaggia facilmente dentro o fuori dalle cellule, hanno usato un analogo che riesce a passare meglio attraverso le membrane delle cellule nervose. La strategia ha funzionato, riparando fino a tre quarti delle sinapsi che erano state perse, prevenendo al contempo un ulteriore declino.
"Il succinato non è un composto che le persone possono ora prendere come trattamento, ma è la prova del principio che puoi ri-energizzare il ciclo di Krebs", afferma Lipton. "La bellezza dello studio è che siamo riusciti a dimostrarlo nelle cellule nervose viventi derivate da pazienti di MA, ma dobbiamo ancora elaborare un composto molto migliore per arrivare a un farmaco efficace che gli umani possono assumere".
Lipton ha una storia di sviluppo di farmaci approvati dalla FDA per il MA, come il Namenda®, e ammette che qui è necessario molto più lavoro per produrre un farmaco che conservi l'energia aggiuntiva, che sia sicuro ed efficace nell'uomo.
Il suo laboratorio continuerà a lavorare sul ciclo mitocondriale di Krebs come bersaglio terapeutico promettente nella speranza di poter ripristinare la connettività neuronale nei pazienti con MA, fermando così la progressione della malattia e migliorando la funzione cognitiva.
Fonte: Scripps Research Institute (> English) - Traduzione di Franco Pellizzari.
Riferimenti: AY Andreyev, [+11], SA Lipton. Metabolic Bypass Rescues Aberrant S‐nitrosylation‐Induced TCA Cycle Inhibition and Synapse Loss in Alzheimer's Disease Human Neurons. Advanced Science, 2024, DOI
Copyright: Tutti i diritti di testi o marchi inclusi nell'articolo sono riservati ai rispettivi proprietari.
Liberatoria: Questo articolo non propone terapie o diete; per qualsiasi modifica della propria cura o regime alimentare si consiglia di rivolgersi a un medico o dietologo. Il contenuto non rappresenta necessariamente l'opinione dell'Associazione Alzheimer OdV di Riese Pio X ma solo quella dell'autore citato come "Fonte". I siti terzi raggiungibili da eventuali collegamenti contenuti nell'articolo e/o dagli annunci pubblicitari sono completamente estranei all'Associazione, il loro accesso e uso è a discrezione dell'utente. Liberatoria completa qui.
Nota: L'articolo potrebbe riferire risultati di ricerche mediche, psicologiche, scientifiche o sportive che riflettono lo stato delle conoscenze raggiunte fino alla data della loro pubblicazione.









 Associazione Alzheimer OdV
Associazione Alzheimer OdV